Основы лечения, диагностика и профилактика синегнойной палочки (инфекции). Фото
Основы лечения, диагностика и профилактика синегнойной палочки (инфекции). ФотоСвоевременная диагностика синегнойной инфекции основана на идентификации микроорганизма и определение чувствительности к антибиотикам. Адекватное лечение представляет больному шанс на полное выздоровление и предотвращает прогрессирование заболевания.
Учитывая то, что специфическая профилактика синегнойной инфекции широкого распространения не получила, дезинфекция, стерилизация и соблюдение правил личной гигиены являются самыми эффективными способами, предупреждающими распространение инфекции.
Микробиологическая диагностика синегнойной палочки
Диагностика синегнойной палочки проводится поэтапно. В ряде случаев при поражении кожных покровов и ногтей можно установить предварительный диагноз по внешним признакам. Окончательный диагноз устанавливается только после лабораторного исследования, включающего в себя выделение возбудителя (обязательно до начала лечения), его идентификация (обнаружение пигмента, определение биохимических и серологических свойств) и определение чувствительности к антибактериальным препаратам. Общеклинические и инструментальные методы диагностики являются дополнительными.


Рис. 1. Синегнойная инфекция. Язва роговицы.
Предварительная диагностика синегнойной инфекции
Предварительный диагноз инфицирования синегнойной палочкой можно поставить на основании специфического окрашивания ран, перевязочного материала и пораженных ногтей в сине-зеленый цвет. Характерным при поражении является развитие на кожных покровах гангренозной эктимы (см. фото). Заболевание развивается при септицемии у лиц с иммунодефицитом.


Рис. 2. Гангренозная эктима, связанная с бактериемией Pseudomonas aeruginosa.2
Чрезвычайно болезненная язва, с некрозом в центре, окруженная ярко-красным ободком (фото слева). Спустя 2 недели язва увеличилась в размерах, имеет фестончатые края (фото справа).


Рис. 3. Окрашивание повязки на ране (фото слева) и ногтей (фото справа) в сине-зеленый цвет ферментом пиоцианином, который синтезируется синегнойной палочкой.
Материал для лабораторного исследования
Материал, взятый непосредственно из очага поражения, является основным при исследовании больных с подозрением на псевдомонадную инфекцию. Во всех других случаях материалом могут быть испражнения, моча, мокрота, гнойное отделяемое, слизь, экссудат, ликвор, трахеобронхиальные смывы, отделяемое из влагалища или канала шейки матки, желчь и кровь. Материалом для исследования могут стать лекарственные препараты, изготовленные в больницах, смывы с предметов ухода за больными, медицинской аппаратуры и санитарно-гигиенического оборудования.
Бактериологический метод исследования
Бактериологический метод исследования является единственным и самым эффективным при диагностике синегнойной инфекции. Его необходимо использовать еще до начала лечения.
К питательным средам синегнойные палочки нетребовательны. Растут на простых питательных средах. Колонии гладкие, полупрозрачные, окрашиваются в разные цвета (чаще в сине-зеленый), имеют специфический запах карамели, жасмина или винограда.


Рис. 4. Колонии синегнойной палочки: полукруглые (фото слева) и в форме маргаритки (фото справа).


Рис. 5. На фото синегнойные палочки под микроскопом. Окраска по Граму.
При идентификации выделенных культур учитывают следующие свойства возбудителей:
- Рост колоний при температуре 42°С.
- Пигментообразование.
- Образование слизи.
- Симптом радужного лизиса.
- Образование зоны гемолиза.
- (+) результат оксидазного теста.
- Пигментообразование. На плотных средах уже через 24 часа отмечается рост колоний возбудителей. Они слизистые, полупрозрачные, с перламутровым оттенком. От 70 до 80% клинических изолятов синтезируют пигмент пиоцианин, окрашивающий питательную среду в сине-зеленый цвет, что является важным диагностическим признаком. Ряд штаммов продуцируют пигмент пиовердин (флюоресцеин) — пигмент желто-зеленого цвета, пиорубин окрашивает питательную среду в красный или бурый цвета, пиомеланин (меланиновый пигмент) окрашивает питательную среду в черный, коричнево-красный или коричнево-черный цвета, L-оксифеназин дает желтую окраску.
- Температура роста. Рост синегнойной палочки в аэробных условиях происходит даже при температуре 42°С, что используется как дифференциально-диагностический признак.
- Феномен радужного лизиса. При росте возбудителей на плотных средах регистрируется феномен радужного лизиса, который происходит под влиянием спонтанного бактериофага, что является таксономическим признаком.
- Гемолиз. При росте на 5% кровяном агаре вокруг колоний образуется зона просветления (гемолиза), что связано с разрушением эритроцитов.
- Образование слизи. При росте на жидких питательных средах на поверхности образуется серовато-серебристая пленка. По мере старения культур образуется муть, которая со временем опускается сверху вниз.
- Оксидазный тест. Синегнойные палочки синтезируют цитохромоксидазу. Оксидазный тест является ведущим при идентификации возбудителей. При положительном результате тест-полоска окрашивается в сине-фиолетовый цвет.


Рис. 6. Посев на синегнойную палочку. Окрашивание питательной среды ферментом пиоцианином в сине-зеленый цвет.


Рис. 7. Синегнойные бактерии синтезируют слизь (внеклеточное крахмалоподобное вещество).


Рис. 8. Зона просветления вокруг колоний возбудителей.


Рис. 9. Положительный и отрицательный оксидазный тест.
Определение чувствительности Pseudomonas aeruginosa
Антибиотикотерапия синегнойной инфекции проводится только с учетом чувствительности возбудителей к антибактериальным препаратам.


Рис. 10. Определение чувствительности выделенного возбудителя к антибиотикам. Методика стандартных дисков. Чем больше зона просветления, тем чувствительнее бактерии к антибиотикам.
Серологическая идентификация и определение сероваров
Серологическая идентификация и определение сероваров возбудителей проводится при наличии соответствующих типов сывороток путем постановки реакции агглютинации с определением антигенов: моноспецифических Н-антигенов и групоспецифичного О-антигена. Данные виды исследований на сегодняшний день требуют дальнейшего совершенствования.
к содержанию ↑Лечение
Лечение синегнойной инфекции включает в себя этиотропную терапию, применение патогенетических и симптоматических средств. Этиотропная терапия направлена на борьбу с инфекцией и включает в себя применение следующих групп лечебных средств:
- Антибиотики (с учетом чувствительности возбудителей).
- Плазма из крови больных, иммунизированной поливалентной корпускулярной синегнойной вакциной (иммунная гомологичная плазма, иммуноглобулин).
- Гетерологичный антисинегнойный иммуноглобулин для местного лечения.
- Синегнойный бактериофаг для лечения ожогов и гнойных инфекций кожи.


Рис. 11. На фото синегнойная инфекция мягких тканей стопы до и после лечения.
Антибиотики от синегнойной палочки
Из-за множественной резистентности (устойчивости) синегнойная инфекция тяжело поддается лечению. Причиной этого является передавая по наследству плазмидами (молекулы ДНК) резистентности к целому ряду антибактериальных препаратов (до 20). Механизмы устойчивости:
- Блокада транспортировки препарата внутрь клетки (внутриклеточной мишени).
- Инактивация препарата (антибиотика) ферментами бактериальной клетки — бета-лактамазами, апетилтрансферазами и нуклеотидазами.
- Активное выведение препаратов из клетки возбудителя.
Наиболее активные антибиотики против синегнойной палочки:
- β-лактамные антибиотики (пенициллины, карбапенемы, цефалоспорины и монобактамы). В порядке убывания:
Карбапенемные антибиотики (Имипенем и Меропенем) обладают наибольшей природной активностью в отношении Pseudomonas aeruginosa.
Цефалоспорины IV поколения (Цефепим) и III поколения (Цефтазидим, Цефоперазон).
Монобактамы (Азтреонам)
Пенициллины антипсевдомонадные: уредопенициллины (Пиперациллин, Пиперациллин/Тазобактам) и карбоксипенициллины (Карбенициллин, Тикарциллин, Тикарциллин/Клавуланат).
- Аминогликозиды (Амикацин).
- Фторхинолоны (Ципрофлоксацин, Левофлоксацин). Чувствительность к ним быстро сменяется на устойчивость.
При лечении синегнойной инфекции β-лактамные антибиотики часто применяются в сочетании с Амикацином или Ципрофлоксацином. Наибольшую чувствительность Pseudomonas aeruginosa регистрируется в отношении Меропенема и Амикацина.
Практически не встречается устойчивости бактерий к Полимиксину.
Лечение синегнойной инфекции достаточно сложное, без адекватного микробиологического контроля малоэффективное. Чувствительность Pseudomonas aeruginosa прогнозируется плохо.


Рис. 12. Синегнойная инфекция наружного слухового прохода.
Бактериофаг против синегнойной палочки
Наряду с применением антибиотиков при лечении синегнойной инфекции используется синегнойный бактериофаг. Иммунологический препарат обладает способностью разрушать (растворять) бактериальные клетки, способствует синтезу иммуноглобулинов, снимает выраженные симптомы заболевания, способствует выздоровлению.
Обязательным условием применения препарата является предварительное определение чувствительности возбудителя. Препарат применяется при разных локализациях воспалительного процесса в виде раствора местно, ректально, вагинально и перорально.
- Местно бактериофаг применяется в виде повязок, орошений, аппликаций и тампонов.
- В плевральную, суставную и брюшную полости бактериофаг вводится через дренажную трубку.
- В полость мочевого пузыря препарат вводится через катетер, в почечную лоханку — через нефростому или цистостому.
- При остеомиелите препарат вводится через дренаж или турунды.
- При гинекологических заболеваниях бактериофаг вводится в полость влагалища и матки.
- При заболеваниях ЛОР-органов раствор бактериофага вводится в полость среднего уха и нос. Препарат используется в виде полоскания, закапывания, промывания, введения смоченных в растворе турунд.
- Детям в возрасте до 6-и месяцев бактериофаг вводится через прямую кишку в виде высоких клизм.
Курс лечения раствором синегнойного бактериофага составляет 5 — 15 дней. В случае возникновения рецидивов заболевания рекомендуется проведение повторных курсов. Бактериофаг разрешено применять вместе с другими препаратами, использующимися при лечении синегнойной инфекции.


Рис. 13. Бактериофаг синегнойной палочки.
Хирургия синегнойной инфекции
В ряде случаев при синегнойной инфекции требуется применение хирургических методов лечения:
- Удаление некротизированных участков тканей.
- Дренирование при скоплении гноя в полостях.
- Лапаротомия с последующей резекцией при некротическом энтероколите.
- Хирургическое лечение при обструкциях мочевых путей.
- Протезирование клапанов сердца при их поражении
Профилактика синегнойной инфекции
Профилактика синегнойной инфекции подразделяется на специфическую и неспецифическую.
Специфическая профилактика
Специфическая профилактика синегнойной инфекции предполагает применение иммунных антигенных препаратов, которые выделяются из различных компонентов самой бактерии, а также с помощью полученных на их основе гипериммунной плазмы и иммуноглобулина. С профилактической целью применяются следующие препараты:
- Пиоиммуноген применяется местно при ожогах.
- Ассоциированная вакцина, в состав которой входят антигены синегнойной палочки, стафилококка и протея.
- Поливалентная корпускулярная синегнойная вакцина.
- Пассивная специфическая иммунизация проводится гипериммунной плазмой.
Неспецифическая профилактика
Учитывая то, что специфическая профилактика сегодня широкого распространения не получила, дезинфекция, стерилизация и соблюдение правил личной гигиены являются самыми эффективными способами, предупреждающими распространение инфекции.
- В больничных условиях необходимо строго соблюдать правила асептики и антисептики. Постоянно проводить контроль за обсемененностью внешней среды.
- Своевременно и правильно обрабатывать раны и ожоговые поверхности.
- Не допускать развитие иммунодефицитных состояний.
- Соблюдать правила личной гигиены.
- Укреплять здоровье.
- В бассейнах и горячих ваннах постоянно контролировать концентрацию хлористых веществ (70,5 мг/л) и норму водородного показателя воды (7,2-7,8).


Рис. 14. На фото синегнойная инфекция — псевдомонадная опрелость.
ССЫЛКИ ПО ТЕМЕ Статьи раздела «Синегнойная инфекция»Самое популярноеПОНРАВИЛАСЬ СТАТЬЯ?
Подпишитесь на нашу рассылку!
Статьи раздела «Синегнойная инфекция» Новые статьи Популярные статьи Похожие статьи О микробах и болезнях © 2020 НаверхСинегнойная инфекция. Pseudomonas aeruginosa (синегнойная палочка)
За всю сознательную жизнь каждый человек на планете подвергается атаке разнообразных вирусов, бактерий. Некоторые опасные гости оставляют после себя ряд неприятных последствий и осложнений, которые проявляются в пожилом возрасте. У каждого патогенного микроорганизма своя роль, задача, все они выявляются по-разному, и, соответственно, специфика лечения у них индивидуальная.
В медицинской практике зафиксировано множество опасных заболеваний, о которых обычный человек даже не догадывается. К таковым относится синегнойная инфекция, вызываемая аэробной неспорообразующей палочкой рода Pseudomonas aeruginosa. Это подвижная бактерия, способная перерабатывать источники углерода в окружающей среде.
Главная особенность заключается в том, что для сохранения жизнедеятельности ей не требуются особые питательные элементы, она отлично адаптируется и размножается в среде с полным отсутствием органических веществ. Может существовать даже в дезинфектантах и развиваться в обычной дистиллированной жидкости.
Основной целью сегодняшней публикации является подробное ознакомление с клинико-эпидемиологическими свойствами этой бактерии, определением методов антибактериальной терапии. Мы расскажем, чем опасны нозокомиальные инфекции, какие влекут патологии, и узнаем особенности альтернативного лечения.
Характеристика
Официальной науке известны около 140 разновидностей грамотрицательных бактерий этого подвида. Основной ареал их обитания – окружающая среда. Возбудитель предпочитает влажную почву, воду, живет внутри растений, в ЖКТ животных и даже людей. Бактерия Pseudomonas aeruginosa отлично себя чувствует при температуре от 37 до 42 градусов, активно размножается и быстро растет.
Патогенный микроорганизм представляет угрозу для человека, устойчив в отношении большинства антибактериальных и антимикробных препаратов. Стоит отметить, что у 10% здоровых людей бактерия обнаруживается на кожных покровах, в паховой области, возле ушных раковин, слизистой носоглотки и в составе микрофлоры кишечника.
Наука предполагает, что риск возникновения опасного заболевания существует, если количество синегнойной палочки превышает допустимые рамки. Наиболее подвержены тяжелым патологическим процессам лица с хроническими болезнями, ослабленным иммунитетом. Подхватить возбудителя можно аэрозольным, пищевым, контактно-бытовым путем. По статистическим данным, чаще всего заражение происходит в лечебном учреждении через медицинское оборудование, необработанные инструменты, растворы, антисептические средства, эндоскопы.
В последнее время внутрибольничные (нозокомиальные) инфекции (ВБИ) весьма актуальны во всем мире. Наиболее восприимчивы к ним маленькие дети, пожилые люди, пациенты со слабой иммунологической реактивностью. Для снижения риска распространения инфекции создаются новые инновационные диагностические и терапевтические методы, инструментальное оборудование, позволяющее выявлять нозологические формы болезни.
Подробнее о внутрибольничных инфекциях
Всемирная организация здравоохранения бьет тревогу по количеству заболевших пациентов, которые пребывали на стационарном лечении в медицинском учреждении. ВБИ, включая Pseudomonas aeruginosa, — серьезная проблема для всего мирового сообщества, зачастую влекущая за собой летальные исходы. Связано это с плохой санитарной обработкой помещений, аппаратуры, наличием скрытой болезни у медработников. Выявляется синегнойная инфекция во внутренних органах, в рваных и гнойных ранах, а также мелких порезах, дыхательных путях, кишечном тракте. В зависимости от локализации возбудителя проявляются характерные симптомы.
Типичные признаки
Патогенный микроорганизм может поражать многие ткани и органы человека, при этом длительный период времени никак себя не выдавать, причиняя значительный урон здоровью. Синегнойная палочка вызывает серьезные осложнения: сепсис, гангренозную эктиму, некроз, менингит и проч. При поражении мочевыделительной системы симптоматика характеризуется резями во время опорожнения пузыря, болевыми ощущениями в области живота, жжением. Многие пациенты самостоятельно ставят себе диагнозы и принимают препараты бесконтрольно.
Крайне опасно для человека обнаружение бактерии в кишечном тракте. Она вызывает дисбактериоз, энтериты, колиты. Появляются интоксикация, сильнейшие боли, нарушение стула, рвота, тошнота. Вырабатываемые микробом токсины разрушают сосуды, поражают клетки печени и провоцируют гемолиз кровяных клеток (эритроцитов). Кишечная палочка синегнойная в запущенной стадии практически не излечивается и создает угрозу для жизни.
Где локализуется возбудитель и что вызывает?
Проникая в организм, синегнойная палочка вызывает вспышки инфекционных и воспалительных заболеваний со стороны мочевой, пищеварительной, дыхательной, легочной систем. Губительному воздействию подвержены ЛОР-органы. Диагностируется синегнойная палочка в ухе, вызывая гнойный отит с примесью крови. Инфекция может проявляться ринитом, хроническим гайморитом, аденоидитом, пневмонией и бронхитом.
А при захвате мочевыводящей системы развиваются уретрит, цистит, пиелонефрит. При ожогах, язвах, гнойных ранах бактерия провоцирует развитие абсцесса и сепсиса. В группу риска входят лежачие пациенты, за которыми не осуществляется должный уход. В результате длительного обездвижения образуются мокнущие пролежни – ворота для Pseudomonas aeruginosa. Существует масса патологий, которые вызывает синегнойная палочка. Терапия их затруднительна и требует максимального контроля со стороны врача.
Зачастую Pseudomonas aeruginosa обнаруживается у людей с диагнозом «острая пневмония». Инфекция может спровоцировать эндокардит, патологию ЦНС и костно-мышечного аппарата. Иногда локальная бактерия переходит в фатальную бактериемию (заражение всего организма), в этом случае прогноз будет удручающим. Нужно сказать, что механизм губительного воздействия этой палочки происходит в два этапа: инвазивный и токсигенный.
Синегнойная палочка у ребенка: насколько опасна?
Мировая педиатрия обеспокоена участившимися случаями появления нозокомиальных инфекций в раннем возрасте. Им подвержены в основном дети с недостаточным весом, недоношенные и ослабленные. Имеются данные о летальных исходах (11%). Локализация возбудителя зачастую распространяется на кишечный тракт, дыхательные пути и ЛОР-органы. В каждом отдельном случае требуется индивидуальная комплексная терапия. В обязательном порядке ребенок отправляется в инфекционное отделение.
Клиническая картина у детей
Все чаще регистрируются случаи больных пневмонией, которую провоцирует грамотрицательная бактерия рода Pseudomonas. Симптоматика ярко выраженная: высокая температура, изнуряющий кашель с вязкой и обильной мокротой. Через сутки выделяется гной, наблюдается одышка и кислородное голодание.
На рентгенологическом снимке видны значительные изменения в легких. Требуется незамедлительное лечение. Не менее опасно, когда синегнойная палочка у ребенка проникает в ЖКТ. Появляются сильнейшая рвота, диарея с примесью слизи и гноя, болевой синдром в животе.
Отмечаются серьезные нарушения микрофлоры кишечника, судороги, тяжесть и урчание, малыш очень быстро теряет запасы жидкости, что грозит обезвоживанием. Инфекция проявляется у детей, страдающих муковисцидозом (кистозным фиброзом) — наследственным заболеванием. На фоне этой патологии защитные антитела не борются с чужеродным агентом, мало помогают и антибиотики, вследствие этого бактерия молниеносно прогрессирует, постепенно убивая живой организм.
Диагностические мероприятия
Синегнойная инфекция по визуальному осмотру и общему анамнезу не определяется. Обязательно берется бактериологический посев на выявление палочки (гнойное содержимое, слизь, моча, кровь), и проводится серологическое исследование. На основе полученных результатов выявляются антитела возбудителя, выносится окончательная оценка, подбирается и устанавливается терапия. Культурная диагностика не представляет трудностей и производится в кратчайшие сроки.
Синегнойная инфекция: как лечить патологию?
Еще лет 20 тому назад бактерия не поддавалась терапии, смертельные исходы случались гораздо чаще, нежели в 21 веке. Науке удалось достичь максимальных результатов в борьбе с этим коварным недугом. Ученые изобрели мощные антибактериальные средства, блокирующие патогенные микроорганизмы. К таковым относятся:
— фторхинолоны;
— карбапенемы;
— уреидопенициллины;
— монобактамы.
К глубокому сожалению, данный вид патогенных бактерий мутирует, развивает резистентность даже к усовершенствованным антимикробным медикаментам. Чтобы полностью подавить инфекцию и исключить рецидив, целесообразно начинать терапию на ранней стадии развития болезни. Лечится длительное время (не меньше двух недель) синегнойная палочка. Антибиотики назначаются после сдачи необходимых анализов и подтверждения диагноза. Только врач определяет, какие препараты уместны в том или ином случае.
Обычно назначается ступенчатое (попеременное) лечение при помощи антибиотиков: внутривенно, затем внутримышечно. При поражении мочевыделительной системы обязательно используются инстилляции (вводится катетер с лекарством в пузырь). Если инфекция затронула слизистые оболочки и кожные покровы, то накладываются компрессы, примочки, марлевые повязки, делаются полоскания, впрыскивания.
При необходимости производится хирургическое иссечение омертвевшей ткани, подобное отмечается при пролежнях. Неотъемлемой частью терапии является укрепление защитных сил организма. Лучшим на сегодняшний день фильтратом фаголизата бактерии фармацевтика считает бактериофаг синегнойной палочки. Это современный антибактериальный раствор, купирующий патогенные клетки. Подходит для лечения всех локализаций. Используется ректально, перорально и местно. Повышает синтез иммуноглобулина, снимает выраженные симптомы и помогает выздоровлению. После полного курса лечения и ликвидации клинической картины, примерно через десять суток, необходимо провести повторный анализ для выявления возбудителя. Если посев вновь покажет положительную реакцию, назначается новый антибиотик.
Дополнительные методы терапии
Лечение синегнойной инфекции целесообразно сочетать с общеукрепляющими, пробиотическими и гомеопатическими средствами, но только под чутким контролем доктора. В определенной дозировке назначается витаминно-минеральный комплекс, направленный на укрепление иммунитета. В период терапии необходимо соблюдать рациональное питание, исключив вредные углеводы, жиры. Меню должно быть легким, обогащенным белками, свежими овощами и фруктами.
Альтернативные методы избавления от инфекции
Без консультации и рекомендации специалиста крайне опасно назначать те или иные лекарственные травы. Неизвестно, какую они вызовут реакцию в вашем случае. Настоятельно советуем не рисковать собственным здоровьем. Некоторые практикующие врачи и гомеопаты назначают в комплексе растительные компоненты. Если выполнять все предписания и следовать советам медицинских работников, то можно навсегда попрощаться с диагнозом «синегнойная палочка».
Народные средства, такие как полевой хвощ, листья осины, масло чайного дерева, ромашка, помогают в устранении воспалительного процесса и облегчают течение болезни. Хорошо зарекомендовал себя продукт пчеловодства – прополис, обладающий антибактериальными, антисептическими свойствами. Издавна из него изготавливают отвары, настои, мази для местного использования. Опишем несколько народных рецептов.
- В равных пропорциях заварить листья полевого хвоща (либо подорожника) и осины крутым кипятком. Выпивать ежедневно по 30 г (две столовые ложки) перед приемом пищи, только в разбавленном виде (с чаем или водой). Можно полоскать гортань, промывать носовые пазухи. Домашнее снадобье обладает антимикробным, противовоспалительным и дезинтоксикационным воздействием.
- Народные знахари рекомендуют употреблять натуральные антибиотики для лечения разных недугов. К таковым относят масло чайного дерева, которое реализуется в аптечной сети. Следует соединить каплю этой жидкости с десертной ложкой оливкового масла. Выпивать раз в сутки, запивая водой.
- На столовую ложку ягод калины взять два стакана кипятка. Настоять около часа, пока раствор не приобретет насыщенный цвет. Употреблять по 100 мл четыре раза в сутки. Аналогичный отвар делается из плодов шиповника. Настаивается в термосе и пьется как чай.
- Делаем целебный противоинфекционный настой из пяти сушеных либо свежих цветков календулы и 250 мл крутого кипятка. Смесь настаивается в течение часа. В остывший раствор добавляем большую ложку спиртовой настойки прополиса. Принимать трижды в сутки по 50 граммов. Сочетание двух лечебных растительных компонентов стимулирует иммунобиологические процессы, оказывает губительное влияние на патогенных микробов, замедляет их рост и развитие. Вдобавок такой отвар проявляет анестезирующее и фунгицидное действия.
Помните, что альтернативные методы лечения являются дополнением к медикаментозной терапии и не смогут самостоятельно предотвратить инфекцию. Они всего лишь направлены на укрепление иммунитета и уменьшение воспаления. Необходимо четко понимать и знать о противопоказаниях тех трав и растений, которые принимаете.
О профилактике
Синегнойная палочка (инфекция) весьма распространена в окружающей среде и может колонизировать во внутренние органы человека, нанося огромный вред. Чтобы обезопаситься, необходимо следовать негласным правилам, соблюдать элементарную гигиену. Проще подхватить бактерию в больничной обстановке, нежели от другого человека. При подозрении на источник инфекции следует провести посев у всех членов семьи, проживающих в одной квартире.
Первичная и главная профилактика заключается в контроле за здоровьем, а точнее иммунной системой. Обеспечивайте свой организм сбалансированным пищевым сырьем, всегда тщательно мойте руки в мыльном растворе после садовых работ, прогулки. Пользуйтесь влажными салфетками на улице, когда хотите перекусить.
Для борьбы с возбудителем медицинские работники должны следить за чистотой рук, помещения и оборудования. Обязательно подвергать стерилизации эндотрахеальные трубки, обрабатывать специальными растворами катетеры. Для исключения инфекции в горячих ваннах и бассейнах постоянно контролировать норму водородного показателя воды (7,2-7,8) и концентрацию хлористых веществ (70,5 мг/л).
Все найденные источники бактериального загрязнения в медицинских учреждениях должны незамедлительно уничтожаться. Пациентов с подозрительными симптомами необходимо своевременно обследовать и помещать в инфекционное отделение во избежание распространения патологии. Таким образом удастся минимизировать случаи заражения и правильно скорректировать лечение.
Каковы последствия?
Прогноз напрямую зависит от наличия сопутствующих патологических процессов. Результаты терапии будут положительными при применении ряда антибактериальных препаратов широкого действия. Синегнойная инфекция губительно влияет на многие жизненно важные функции, в особенности на детский организм. В некоторых случаях после длительного лечения и ликвидации основных проявлений через определенный промежуток времени симптоматика может вновь повториться или обостриться на фоне имеющихся патологий.
При подозрительных признаках ухудшения общего состояния здоровья не поленитесь пройти обследование, хотя бы сдать биохимический анализ крови и мочу. Если полученным результатам вы не доверяете, проконсультируйтесь у нескольких специалистов по тревожащей проблеме. Уделяйте своему здоровью максимальное внимание, всегда прислушивайтесь к сигналам, которые подает организм.
Каждое заболевание имеет характерные признаки, которые в основном возникают на острой стадии, затем стихают. Как известно, латентная форма свидетельствует о том, что патология перешла в хроническую форму. В этом случае терапия будет затруднительной, займет немало времени и сил. Никогда не сдавайтесь, боритесь с недугами, окружайте себя положительными эмоциями, избавляйтесь от депрессии и тоски. Путь к крепкому здоровью лежит через профилактику. Помните об этом и не болейте!
Синегнойная палочка | Компетентно о здоровье на iLive
Факторы патогенности синегнойной палочки
Одним из главных факторов патогенности синегнойной палочки и других псевдомонад является О-антиген — липополисахарид клеточной стенки, механизм действия которого такой же, как у других грамотрицательных бактерий.
P. aeruginosa обладает разнообразными факторами патогениости, которые вовлечены в развитие синегнойной инфекции. Среди наиболее важных из них выделяют следующие.
Факторы адгезии и колонизации — пили iV типа (фимбрий) и внеклеточная (экстрацеллюлярная слизь) P. aeruginosa.
[26], [27], [28], [29], [30], [31], [32], [33], [34]
Токсины
ЛПС наружной мембраны клеточной стенки P. aeruginosa обладает свойствами эндотоксина и участвует в развитии лихорадки, олигурии, лейкопении у больных.
Экзотоксин А синегнойной палочки является питотоксином, который вызывает глубокие нарушения клеточного метаболизма в результате подавления синтеза белка в клетках и тканях. Подобно дифтерийному токсину, он является АДФ-рибозилтрансферазой, которая ингибирует фактор элонгации EF-2 и поэтому вызывает нарушение синтеза белка. Также доказано, что экзотоксин А наряду с протеазой подавляет синтез иммуноглобулинов и вызывает нейтропению. Экзотоксин А продуцируется в неактивной форме в виде протоксина и активируется при участии различных ферментов внутри организма. Экзотоксин А обладает протективными свойствами, i.e. антитела к нему защищают клетки хозяина от его повреждающего действия, а также препятствуют развитию бактериемии и синегнойного сепсиса.
Экзотоксин S (экзотзим S) обнаруживается только у высоко вирулентных штаммов синегнойной палочки. Механизм его повреждающего действия на клетки пока неясен, однако известно, что инфекции, обусловленные экзоэнзим-3-продуцирующими штаммами синегнойной палочки, нередко заканчиваются летально. Экзотоксины А и S нарушают также активность фагоцитов.
Лейкоцидин также является цитотоксином с выраженным токсическим воздействием на гранулоциты крови человека.
Энтеротокин и факторы проницаемости играют определенную роль и развитии местных тканевых поражений при кишечных формах синегнойной инфекции, вызывая нарушения водно-солевого обмена.
Ферменты агрессии
P. aeruginosa продуцирует гемолизины двух типов: термолабильную фосфолипазу С и термостабильный гликолипид. Фосфолипаза С разрушает фосфолипиды в составе сурфактантов на альвеолярной поверхности легких, вызывая развитие ателектазов (бронхоэктазов) при патологии респираторного тракта.
Нейраминидаза также играет важную роль в патогенезе бронхо-легочных заболеваний синегнойной этиологии и муковисцидоза, так как участвует в колонизации муцина респираторного тракта.
Эластаза, а также другие протеолитические ферменты синегнойной палочки и экзотоксин А вызывают кровоизлияния (геморрагии), деструкцию тканей и некроз в очагах поражения при инфекциях глаз, пневмонии, септицемии синегнойной этиологии.
[35], [36], [37], [38], [39], [40], [41], [42]
Резистентность псевдомонад
P. aeruginosa характеризуется довольно высокой устойчивостью к антибиотикам, что объясняется плохой проницаемостью наружной мембраны этих бактерий вследствие врожденного дефекта поринов, а также способностью бактерий синтезировать пенициллиназу.
P. aeruginosa сохраняет жизнеспособность в условиях почти полного отсутствия источников питания: она хорошо сохраняется в пресной, морской и даже дистиллированной воде. Доказано также, что культуры синегнойной палочки могут сохраняться и даже размножаться в растворах дезинфицирующих средств (например, фурациллина), предназначенных для хранения катетеров и различных медицинских инструментов, промывания ран в ожоговых и хирургических стационарах.
В то же время P. aeruginosa чувствительна к высушиванию, действию хлорсодержащих дезинфицирующих препаратов и легко инактивируется при воздействии высоких температур (при кипячении, автоклавировании).
Болезни птиц вызываемые Pseudomonas spp. и Aeromonas spp..
Псевдомоноз и аэромоноз птиц
Две грамотрицательные палочки Pseudomonas aeruginosa и Aeromonas hydrophila относятся к разным родам, тем не менее, они приводят к заболеваниям птиц, имеющим схожую симптоматику и патогенез — поэтому, с клинической точки зрения, эти возбудители болезней птиц рассматриваются одновременно. Оба возбудителя часто обнаруживаются во влажной среде (они хорошо развиваются как в холодной воде водоемов, так и в горячей водопроводной воде).
Микробиологические свойства и характеристики возбудителей
Pseudomonas aeruginosa: подвижная, аэробная, грамотрицательная, оксидаза-положительная, неспорообразующая палочка размером 1.5–3х0.5–0.8μm. Бактерии чаще располагаются одиночно, изредка организуясь в короткие цепочки. На питательных средах образует водорастворимый пигмент, содержащий флуоресцеин и пиоцианин.
Псевдомонады в нативном мазке помета ткачика (темнопольная микроскоскопия), хорошо видна подвижность этих бактерий.
Aeromonas hydrophila — коккобацилла с закругленными концами 1,0-3,0х0,3-1,0μm. Передвигается с помощью полярного жгутика. Имеет капсулу. Может расти при низких температурах вплоть до 4 °С.
Обе бактерии растут на обычных питательных средах и приводят к β-гемолизу эритроцитов. Культуры Ps.aeruginosa — имеют характерный сладковатый запах. Ae.hydrophila — обладает выраженной протеолитической активностью, приводящей к появлению запаха гнилого мяса; при культивации на питательных средах Эндо или МакКонки — возбудитель легко может быть спутан с кишечной палочкой.
Патогенность
Обе бактерии могут инфицировать большое количество разных животных, в том числе человека и все виды птиц. Инфекции, вызываемые Pseudomonas spp., называются псевдомонозами. Aeromonas spp. — вызывают аэромонозы птиц. Особенно часто аэромонозом и псевдомозом болеют водоплаваюшие птицы, вероятно из-за частого контакта с этими возбудителями в водной среде. В зоопарках псевдомонозом и аэромонозом часто болеют пингвины, журавли и лебеди.
Неправильно приготовленное пророщенное зерно или проростки, загрязненные купалки, поилки, увлажнители, мойки воздуха, пульверизаторы, водопроводные фильтры — могут являться источником
У дворовой птицы (кур, гусей уток, цесарок, павлинов и фазанов) псевдомонады вызывают локальные и системные инфекции, особенно опасные для цыплят. Отмечена вертикальная, трансовариальная передача бактерий и поражение эмбрионов, а также только что вылупившихся птенцов.
Псевдомонады рассматриваются как оппортунистические возбудители вторичных инфекций, приводящие к развитию болезней дыхательной системы, синуситов, кератитов и кератоконьюнктивитов или септицемии. У эмбрионов и только что вылупившихся птенцов синегнойная палочка вызывает омфалит («воспаление пупка») или воспаление желточного мешка.
Псевдомонады часто осложняют течение вирусных инфекций, других бактериальных инфекций, микоплазмоза, грибковых болезней птиц. Заболеваемость и смертность обычно колеблется в пределах 2-10%, хотя для некоторых штаммов может достигать 100%.
Псевдомонады в условиях высокой влажности способны разрушать кутикулу яиц, увеличивая этим риск заражения эмбриона другими бактериальными (в частности сальмонеллезом) или грибковыми инфекциями (аспергиллезом).
Возбудители псевдомонозов
Pseudomonas aeruginosa (известная как синегнойная палочка) — наиболее частый возбудитель псеводомоноза птиц. Вирулентность возбудителя сильно отличается в зависимости от штамма. Смертность цыплят при заражении в желточный мешок колебалась от 0 до 90%.
P.fluorescens — вызывает респираторные инфекции у канареек, ткачиков, волнистых попугаев, цыплят. Известно об инфицировании эмбрионов индюшек после обработки яиц в растворе антибиотиков, загрязненном этой бактерией, перед закладкой в инкубатор .
P.stutzeri — была выделена от цыплят больных воспалением легких. Однако при экспериментальном заражении этим возбудителем отмечался низкий уровень смертности кур.
Burkholderia [Pseudomonas] pseudomallei. К мелиоидозу восприимчивы куры, но эта болезнь не принимает характер эпидемий в птицеводческих хозяйствах.
Возбудители аэромонозов
Aeromonas spp. — обычные «обитатели» пресных водоемов и возбудители инфекции рыб и других водных животных, в том числе водоплавающих и околоводных птиц.
Aeromonas spp. и E.coli — наиболее частые возбудители, выделяемые у гусей, больных некрозом фаллоса. Также, аэромонады относятся к частым возбудителям, вызывающим внутрияйцевую гибель эмбрионов птиц или смерть только что вылупившихся птенцов. У страусов отмечена зависимость от контаминации яиц аэромонадами и снижением выводимости птенцов.
Ae.hydrophila — выделяли от уток с сальпингитом (воспаление яйцевода), септицемией, аэросаккулитом (воспаление воздушных мешков) и с гранулематозным воспалением солевых желез.
Ae.formicans — выделяли из суставов уток, больных артритом.
Патогенез
Некоторые штаммы синегнойной палочки и аэромонад продуцируют большое количество экзотоксинов, включая: гемолизины, эластазы, протеиназы, лектиназы — все эти факторы патогенности приводят к повреждению клеток хозяина, отеку, кровоизлияниям и некрозу тканей.
Штаммы Ae.hydrophila, синтезирующие ацетоин (положительная реакция Фогес-Проскауера), особенно токсичны для птиц. Аеромонады колонизируют кишечник птиц благодаря лиополисахаридному О-антигену, факторами патогенности являются многочисленные цитотоксины патогенные, в том числе и для человека.
Клинические признаки и патологический процесс
Септицемия
Вирулентные штаммы псевдомонад и аэромонад приводят к развитию септических инфекций, сопровождающихся такими неспецифичными признаками болезней птиц как: понос (диарея), отказ от еды (анорексия), вялость, взъерошенность оперения, обезвоживание, диспное (нарушение нормального ритма дыхания) и внезапная гибель птицы в течение 24-72 часов. При поражении почек развивается хромота, частичный или полный парез лап.
При развитии хронической формы инфекции может развиваться: сальпингит, гепатит, намины и попутный клапанный эндокардит, который часто отмечают у куриных (Galliformes), гусиных (Anseriformes), орлов (Aquila), эму (Dromaius), казуаров (Casuarius), фламинго (Phoenicopteridae), попугаев ара (Ara).
Болезни репродуктивной системы
Pseudomonas spp. выделяли от взрослых кур-несушек с сальпингитом и оофоритом; от гусей, страдающих инфекцией половых путей.
Болезни дыхательной системы
Респираторная форма инфекции сопровождается односторонним или двусторонним синуситом, ринитом, синдромом «вздутой головы», ларингитом, отеком восковицы, чиханием, обильными выделениями слизи из ноздрей. Без лечения развивается нисходящий бронхит, пневмония и аэросаккулит.
У фазанов при респираторной форме инфекции отмечается гетерофильный экссудат в глотке и очаговая пневмония. У страусят при аналогичной форме заболевания отмечали псевдодифтеритные наложения и гранулематозные очаги поражения в верхних дыхательных путях и в пищеводе. Инфекция протекала с большой смертностью страусов.
У взрослых попугаев амазонов (Amazona) и ара (Ara) P.aeruginosa вызывает развитие хронического ринита, признаками которого является периодические выделения из ноздрей (из одной или из обеих) и чихания. В остальном попугаи выглядят здоровыми, сохраняют хороший аппетит и активность.
Такая болезнь может длиться годами. Я наблюдал амазона Мюллера (Amazona farinosa) с хроническим ринитом, владельцы которого на протяжении 5 лет отказывались от обследования попугая, потому что насморк и чихания периодически прекращались. Птица «внезапно» погибла. При вскрытии из носовой полости и печени была выделена чистая культура синегнойной палочки. Из сопутствующих признаков было обнаружено: утолщение стенок воздушных мешков, умеренная спленомегалия и нефроз.
У уток инфицирование носовых желез псевдомонадами приводит к гранулематозному адениту. Сопутствующими признаками и поражениями являются: отек подкожной клетчатки, кровотечение, скопление экссудата в полостях пораженных суставов, серозит схожий с поражениями при колисептицемии, аэросаккулит, перикардит, перигепатит, пневмония, увеличение печени и очаговый некроз печени, селезенки, почек, головного мозга, конъюнктивит, синусит и кератит.
Болезни кожных покровов
При поражении кожи развивается некротизирующий дерматит, протекающий с развитием хорошо заметного отека кожи вокруг пораженного участка. У индеек, канареек, перепелов, голубей, ткачиков, какаду, амадин — P. aeruginosa и Aeromonas spp. выделяли из очагов целлюлита.
Болезни суставов
Псевдомонады являются наиболее часто выделяемой бактерией из пораженных суставов лап у бройлеров, не способных стоять на лапах.
При развитии септического артрита кожа вокруг пораженных суставов отечная («опухание коленки»), горячая, часто опухают суставы пальцев лап или вся стопа.
Синдром замка челюстей попугаев
Aeromonas spp. и Pseudomonas spp. выделялись от птенцов выкормышей корелл (Nymphicus hollandicus), больных синдромом замка челюстей (lockjaw syndrome of cockatiels) — тризм. Этот синдром встречается у выкормышей разных видов попугаев, но чаще всего поражает корелл в возрасте 3-10 недель. Больные птенцы не могут открыть клюв из-за прогрессирующего некротизирующего миозита челюстных мышц и септического артрита височно-нижнечелюстного сустава. Начальными признаками проблемы может являться ринит и синусит с сопутствующими выделениями из ноздрей попугая. Другими возбудителями, обнаруживаемыми при этом заболевании птенцов, являются: Bordetella avium, Klebsiella spp, Enterococcus spp, Staphylococcus spp, Streptococcus spp и Bacillus spp.
Тризм — тонический спазм жевательной мускулатуры, приводящий к ограничению движений в височно-нижнечелюстном суставе. Является симптомом патологических процессов, возникающих как при непосредственном, так и при рефлекторном раздражении третьей ветви тройничного нерва, участвующей в иннервации жевательных мышц.
Болезни центральной нервной системы
Наряду со стафилококками, сальмонеллами, клебсиеллами и кишечной палочкой — Pseudomonas spp. вызывает поражение центральной нервной системы птиц с развитием менингита, энцефалита и миелита.
При поражении центральной нервной системы одним из признаков болезни может являться искривление шеи («кривошея»), атаксия (неспособность ходить и летать), нарушение координации движения.
Болезни глаз
У инфицированных синегнойной палочкой птиц часто развиваются болезни глаз: кератит, блефарит, коньюнктивит, панфотальмит. Двусторонний панофтальмит у птенцов индеек характеризуется прободением роговицы и факолизом (разрушение хрусталика). Быстрое разрушение тканей глаза связано с активностью протеаз, являющихся факторами патогенности псевдомонад. При гистологическом анализе выявляется большое количество бактериальных клеток в пораженных тканях и вокруг сосудов, включая ткани мозга.
У попугаев краснохвостых жако (Psittacus erithacus) синегнойная палочка вызывает развитие хронического блефарита и кератита. Заболевание может длиться годами — как не прогрессируя, так и осложняясь атрофическим ринитом; ноздри птицы внешне могут оставаться слегка припухшими — что обычно не вызывает у владельца птицы беспокойства. Носовая полость попугая, при этом, заполнена сухими ринолитами.
Омфалит

Омфалит — воспаление желточного мешка, вызванное псевдомонадами и аэромонадами. Омфалит частая проблема утят, гусят, лебедят, журавлят, цыплят, фазанят. У выживших экспериментально зараженных в желточный мешок цыплят — через 14 дней отмечали замедление рассасывание желтка и воспаление стенок желточного мешка. При этом, часто развиваются и неврологические признаки заболевания, такие как: кривошея, неспособность стоять на ногах и потеря ориентации птенцов.
На фото типичные признаки омфалита у водоплавающих птиц, вызванного Р.aeruginosa. Видно сопутствующее «искривление шеи». Источник.
Патологоатомические признаки и гистологические изменения.
При вскрытии больных птиц с острой формой инфекции часто обнаруживаются кровоизлияния на печени, сливной некроз печени, селезенки и почек. Не редко развивается катаральный или геморрагический энтерит с отеком и фибринозным воспалением слизистой кишечника. Не редок асцит (как следствие полиорганной недостаточности).
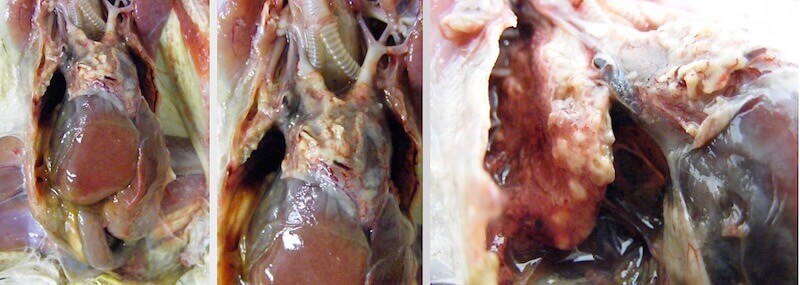
На фото паткартина псевдомоноза обыкновенной сипухи (Tyto alba). Гранулематозная пневмония, гранулематозный перикардит, перигепатит. Pennycott, Tom. (2016). Raptors. Images of pathology (miscellaneous diseases)., 1994-2013. University of Edinburgh. Royal (Dick) School of Veterinary Studies.
Гистологические изменения характеризуются острым воспалением с выраженным флебитом и артериитом. В просвете кровеносных сосудов могут обнаруживаться колонии бацилл и единичные или фагоцитированные бактериальные клетки. В пораженных сосудах формируются тромбы и развивается некроз.
Диагностика
Диагноз ставят после выделения и идентификации возбудителя. Для точной идентификации доступны серологические методы, фаготипирование и аеругиноцинотипирование.
Дифференциальная диагностика
При постановке диагноза псевдомоноз и аеромоноз птиц следует дифференцировать такие болезни птиц, протекающие со сходными клиническими и патологоанатомическими признаками, как: сальмонеллез, эшерихиоз, иерсиниоз, клостридиоз.
Дерматиты необходимо дифференцировать от заболеваний, вызываемых клостридиями, стафилококками, кишечной палочкой, а также от вируса оспы птиц.
Лечение
Лечение псевдомоноза и аэромоноза проводится после определения чувствительности выделенных штаммов к антибиотикам, т.к. данные организмы известны не только своей устойчивостью к антибактериальным препаратам, но и высокой скоростью адаптации к лекарственным препаратам. Некоторые штаммы P.aeruginosa устойчивы практически ко всем антибиотикам, включая аминогликозиды, цефалоспорины, фторхинолоны и карбапенемы.
При лечении псевдомоноза птиц критически важным аспектом является время начала лечения и продолжительность курса антибиотиков; так при хронической форме инфекции гранулематозное воспаление затрудняет проникновение антибиотиков вглубь воспаленных тканей. Также необходимо учитывать, что Pseudomonas spp. и Aeromonas spp., как правило, являются не основной причиной болезни птиц, а осложняют первичные инфекции или неинфекционные заболевания. Поэтому, после начала лечения птицы от вторичных инфекций или после его окончания, следует проводить дополнительную диагностику. Часто псевдомоноз осложняет течение грибковых болезней птиц (аспергиллез, гистоплазмоз, кандидоз) или течение хронических бактериальных инфекций, вызванных микобактериями, иерсиниями, стафилококками.
Меры, направленные на неспецифическое усиление иммунитета птиц, важны для снижения смертности заболевших птиц. Крайне важны обеспечение птиц полноценными рационами, снижение стресса, проведение курсов пробиотических препаратов.
Бактерин, приготовленный из 3х штаммов патогенных для утят аэромонад, успешно применяли в промышленном птицеводстве для снижения смертности уток.
Контроль
Строжайшее соблюдение правил гигиены в инкубаторах и брудера, также и при проведении массовой вакцинации птиц — это главнейшее средство контроля распространения псевдомоноза в хозяйстве или в коллекции птиц. Тщательная очистка и дезинфекция кормушек, поилок, увлажнителей воздуха, пульверизаторов, купалок — очень важна. При проведении вакцинации необходимо использовать только стерильные растворы и оборудование.
Псевдомонады, наряду с другими возбудителями бактериальных инфекций птиц, выделяются из погибших эмбрионов птиц и больных только что вылупившихся птенцов кур, индеек, фазанов, уток и страусов. Птенцы и эмбрионы чаще всего заражаются через недостаточно продезинфицированные перед закладкой в инкубатор инфицированные яйца, впрочем синегнойная палочка (также как и кишечная палочка и клебсиеллы) долго сохраняется в инкубаторах, особенно при большой загрузке хозяйства, когда правильной обработкой инвентаря инкубатория или брудера, а также соблюдением правил гигиены работниками птичника и карантинными мерами — пренебрегают.
Описаны случаи массового заражения цыплят Ps.aeruginosa при вакцинировании от болезни Марека. У птиц развился дерматит в месте инъекции вакцины, которую вводили в верхнюю часть шеи, подкожно. Проблема была связана с тем, что вакцину разводили раствором антибиотиков, который был приготовлен с нарушением правил гигиены и был контаминирован синегнойной палочкой. Далее вакцинированные/инфицированные птицы контактировали с интактными птицами разных возрастов, что привело к распространению инфекции на все хозяйство.
В авиариях и коллекциях птиц вспышка псевдомоноза происходит после заноса синегнойной палочки с грязной водой или немытыми овощами и фруктами. Необходимо тщательно следить за чистотой питьевой воды. Как и при других бактериальных инфекциях птиц — хорошей профилактикой развития болезни является использование нескольких наборов кормушек и поилок, которые сменяются в течение дня (один набор используется, второй сохнет после мытья).
Т.к. Ae.hydrophila особенно активно развиваются при повышении температуры воды в прудах выше 20С, то для предупреждения развития массового мора птицы рекомендуется убирать водоплавающую птицу с непроточных прудов на этот период.
Меры профилактики болезней птенцов
Часто, при несоблюдении киперами правил гигиены, страдают птенцы попугаев. Так, например, в начале 2017 года произошла вспышка псевдомоноза на станции разведения вымирающих золотистобрюхих травяных попугайчиков (Neophema chrysogaster) — за одну ночь погибло 16 птенцов (всего на станции находится 136 попугайчиков). Причина — загрязненная вода, которую применяли для разведения смесей для выкармливания птенцов.
Чтобы избежать заражения выкармливаемых птенцов попугаев и певчих птиц — рекомендуется использовать одноразовые перчатки при любом контакте с птенцами, а также в процессе приготовления смесей для выкормышей. Насекомоядные птицы, птенцы певчих и врановых птиц могут заражаться синегнойной палочкой через размороженных насекомых, в которых псевдомонады развиваются даже при хранении в холодильнике. Нельзя скармливать птенцам врановых, хищных птиц, пингвинов, сов и журавлей — рыбу с признаками краснухи (у рыб Aeromonas hydrophila вызывает инфекцию с характерными язвенными поражениями кожи или с развитием вздутия живота из-за асцита).
У попугаев выкормышей корелл, жако, какаду, амазонов, инфицированных на ранних стадиях развития, остатки желточного мешка сохраняются на долгие годы, вызывая развитие гранулематозного аэросаккулита и энтерита, которые имеют тенденцию осложняться аспергиллезом. Своевременно выявить проблему позволяет диспансеризация птиц, т.к. общие признаки болезни попугая могут оставаться незаметными для владельцев ручных выкормышей из-за их чрезмерной привязанности к человеку и привычного отсутствия адекватной физической активности (т.е. владельцы больной птицы не знают насколько активными должны быть попугаи и принимают «ласку» за норму поведения попугая).
Устойчивость к дезинфицирующим препаратам
После выделения Pseudomonas spp. в хозяйстве или из инкубатора следует проводить тест на чувствительность не только к антибиотикам, но и к дезинфектантам, т.к. многие штаммы синегнойной палочки устойчивы к хлоргексидину. Резистентные штаммы синегнойной палочки выживают при обработке холодными растворами хлоргексидина — это надо принимать во внимание при дезинфекции оборудования для эндоскопии птиц.
Растворы на основе аммиака и его производных были не эффективны при высоких концентрациях P.aeruginosa в брудере, однако при низких концентрациях возбудителя (когда у птенцов не наблюдалось клинических признаков инфекции) такие растворы значительно снижали количество бактерий. Комбинация аммониевых дезинфицирующих растворов и ЭДТА снижала количество бактерий в воздухе помещений и не влияла на выводимость и выживаемость цыплят. Однако надо помнить, что повышенная концентрация аммиака в помещениях с птицами — способствует увеличению восприимчивости птиц к другим инфекционным заболевания, таким как колибактериоз и сальмонеллез.
Зооантропонозное значение
Pseudomonas spp. и Aeromonas spp. — вызывают различные заболевания у человека, что потенцильно говорит о возможной передаче инфекции от человека к птицам и от птиц к человеку, однако публикаций о заражении человека от птиц не обнаружено. Передача возможна контактным путем через грязные руки, слюну человека, инвентарь, помет птиц и воздушно капельным путем.
Примерно 13% инфекций человека, вызываемых P.Aeruginosa, связаны со штаммами, устойчивыми к нескольким классам антибиотиков.
Козлитин В.Е.
Использованная литература:
1. Avian medicine: principles and applications. Ritchie, Harrison and Harrison. 1994. Wingers Publishing, Inc., Lake Worth, Florida
2. Pathology of pet and aviary birds. Robert E. Schmidt, Drury R. Reavill, David N. Phalen.— 1st ed. © 2003 Iowa State Press A Blackwell Publishing Company
3. Большая медицинская энциклопедия / Гл. ред. Б.В.Петровский. — 3-е изд.. — М.:: Советская энциклопедия, 1985.
4. Handbook of avian medicine. Second edition. edited by T.N. Tully. Jr., G.M. Dorrestein. A.K. Jones. © 2000 Saunders elsevier.
5. Diseases of poultry/editor-in-chief, Y.M. Saif ; associate editors, A.M. Fadly … [et al.].—12th ed. © 2008 Blackwell Publishing
6. http://www.abc.net.au/news/2017-01-24/infection-kills-16-endangered-orange-bellied-parrots/8205046
7. Заглавное фото: 3D изображение мультирезистентной к анитибиотикам Pseudomonas aeruginosa, автор рисунка James Archer
Вконтакте
Одноклассники
LiveJournal
Мой мир
Что такое синегнойная палочка? (с иллюстрациями)
Pseudomonas aeruginosa — условно-патогенные бактерии, обитающие в почве, воде и даже в таких средах, как гидромассажные ванны. Для большинства здоровых людей эти бактерии редко представляют проблему. Иногда у людей развиваются такие состояния, как сыпь в горячей ванне и уши пловца, которые могут быть связаны с контактом с этими микробами. Эти состояния иногда могут исчезнуть без лечения или с минимальным лечением, например, с антибиотиками для ушей пловца.
Бактерии Pseudomonas aeruginosa.К сожалению, Pseudomonas aeruginosa намного опаснее для определенных групп населения, в том числе для людей со слабой иммунной системой, пожилых людей и тех, кто находился в больнице на длительное время.Люди с муковисцидозом и СПИДом часто умирают от инфекций, вызванных бактериями. Те, кто прошел химиотерапию, перенесли трансплантаты или имеют какое-либо из множества иммуносупрессивных состояний, гораздо больше подвержены риску развития бактериальных инфекций из-за синегнойной палочки, а поскольку эти бактерии относительно устойчивы к большинству антибактериальных препаратов, инфекция может быть смертельной. особенно, когда это становится инфекцией легких или кровотока.
Люди с муковисцидозом часто умирают от инфекций, вызываемых синегнойной палочкой.Врачи и медицинские исследователи часто называют эти бактерии сине-зелеными гнойными и / или грамотрицательными бактериями. Первая ссылка относится к гною, который может иметь от синего до зеленого цвета, а вторая относится к методу Грама для окрашивания бактерий, чтобы определить, какой это тип. Когда окрашиваются образцы грамотрицательных бактерий, особенно тех, которые считаются аэробными, они не окрашиваются и обычно проявляются на предметных стеклах под микроскопом в виде розового цвета.Аэробные бактерии относятся к бактериям, которым для выживания нужен кислород, которого Pseudomonas aeruginosa имеет в больших количествах, особенно в больничных условиях.
Ушные капли с антибиотиками часто назначают при инфекциях наружного уха, например, уха пловца.Как уже упоминалось, даже при том, что эти бактерии имеют тенденцию жить повсюду вокруг нас, они наиболее опасны для тех, кто находится в ослабленном физическом состоянии или имеет иммунодефицит. Несмотря на чистоту и безопасность в больнице, бактерии могут активно выжить в основном больничном оборудовании, таком как маски, используемые для подачи кислорода, дыхательные аппараты или катетеры для мочи. Обычно наиболее распространенными инфекциями, вызываемыми бактериями, являются мочевой пузырь, легкие или кровоток. Неспособность вызывать нормальные иммунные реакции на присутствие бактерий может означать, что этот микроб может легко привести к чрезвычайно тяжелым заболеваниям.
Pseudomonas aeruginosa особенно опасна для пожилых людей.Лечение синегнойной палочки обычно проводится внутривенным введением нескольких комбинаций антибиотиков, что, к сожалению, не всегда работает. Однако в этой области есть надежда, которая в конечном итоге может положить конец страданиям, которые могут причинять эти бактерии.Предварительные исследования вакцины против Pseudomonas aeruginosa продолжаются, и хотя эти исследования еще не пришли к выводу, что вакцина, разработанная в настоящее время, является полностью эффективной, первые результаты действительно показывают, что вакцина потенциально может снизить количество инфекций по состоянию на середину 2007 года. Эти ранние результаты не показывают полной защиты от инфекции, но они многообещающие в плане снижения по сравнению с группой плацебо. Такая вакцина действительно могла бы стать благом для медицинского сообщества и всех тех, кто подвергается особому риску заражения опасными для жизни инфекциями, вызванными этой бактерией.
Людям с ослабленной иммунной системой следует принимать меры для предотвращения оппортунистических инфекций, вызванных синегнойной палочкой. .Pseudomonas Aeruginosa
Что такое Pseudomonas Aeruginosa
Pseudomonas aeruginosa — важный с медицинской точки зрения представитель рода Pseudomonas у человека. Это примерно 2-4 мм длиной, неспорообразующие грамотрицательные палочки с полярным жгутиком. Pseudomonas aeruginosa можно отнести к простым питательным средам, которые легко культивируются. На твердых носителях проявляются в основном плоские, ярко-серые, часто слизистые колонии, поверхность часто имеет металлический блеск.
Служат источником углерода Органические соединения Pseudomonas aeruginosa необходимы для использования ими молекулярного кислорода в качестве акцептора электронов. Следовательно, бактерии являются обязательными аэробами. Оптимальная температура повышается до 36 ° C. Рост также происходит при 41 ° C, но невозможен при 4 ° C. В жидкой среде семена растут, образуя так называемую пену преимущественно на поверхности.
Большинство штаммов продуцируют пигмент в соответствующих условиях. Основные цвета — желто-зеленый пиовердин (флуоресцеин) и голубовато-зеленый пиоцианин.Из-за образования пигмента синегнойная палочка появилась раньше, чем сине-зеленые гнойные бактерии (Bacterium pyocyaneum). Термин aeruginosa происходит от латинского слова aerugo (verdigris) от.
Патогенез Pseudomonas Aeruginosa
Pseudomonas aeruginosa из-за своей высокой устойчивости и низкой потребности в питательных веществах в окружающей среде широко распространен. Он есть, особенно во влажных местах, таких как почва и поверхностные воды, на растениях и фруктах, а также в толстой кишке здоровых людей.Влажные семена могут также загрязнить многие участки и продукты в домашних условиях. Сюда входят сантехника, моющие средства, лекарства, косметика и жидкости для хранения контактных линз. Но он также может какое-то время выжить в сухой среде. В больнице, расположенной рядом с санитарно-техническими средствами, зараженными растворами для внутривенного вливания и продуктами крови, в первую очередь вентиляторами и небулайзерами, увлажнителями, диализным оборудованием и жидкостями, важный резервуар экстракорпоральных патогенов с высокой устойчивостью Pseudomonas aeruginosa также требует наличия некоторых дезинфицирующих средств недостаточной эффективности.
В больнице — количество пациентов, инфицированных Pseudomonas aeruginosa, с указанием продолжительности пребывания. Заселение предпочтительно происходит на влажной коже. В реанимации пациенты также часто колонизируют верхние дыхательные пути.
Механизмы патогенности сложны. Факторы вирулентности — это фимбрии, которые опосредуют адгезию к поверхности клетки, а также различные ферменты и экзотоксины, производимые бактериями. Эластаза и протеазы способствуют инвазии, где они поддерживаются гемолизинами (особенно фосфолипазой C), которые вызывают повреждение мембран в клетках ткани.Экзотоксин А, вероятно, самый важный фактор вирулентности, экзофермент S, как известно, отрицательно влияет на белок.
Pseudomonas aeruginosa — наиболее распространенные патогены, вызывающие нозокомиальные инфекции. По данным Системы эпиднадзора за больничными инфекциями (KISS) в Германии, вызвано примерно 10% всех больничных инфекций, вызванных синегнойной палочкой. В большинстве случаев это пневмония, кожные и раневые инфекции и инфекции мочеполовых путей. Во время сепсиса доля, вызванная Pseudomonas aeruginosa, составляет около 3%.Pseudomonas sepsis отягощен самым высоким уровнем смертности среди всех форм сепсиса. Другие болезни — гангренозная эктима, менингит, отит и глазные инфекции.
Инфекции, вызванные Pseudomonas aeruginosa, возникают в основном у пациентов с иммунодефицитом. Поэтому большинство случаев обнаруживается в отделениях интенсивной терапии, ожоговых отделениях и гематологических-онкологических отделениях на станциях. Наркоманы тоже подлые. группа риска вне больницы Pseudomonas aeruginosa играет роль возбудителя только у пациентов с муковисцидозом, бронхоэктазами и большей ролью при урологических инфекциях.
Диагноз Pseudomonas Aeruginosa
Микробиологическая диагностика включает выделение патогена из соответствующих тестовых материалов и биохимическую идентификацию.
Pseudomonas aeruginosa обладает естественной устойчивостью ко многим антибиотикам. Доступные в Германии только бета-лактамные антибиотики Ацилуреидопенициллин [пиперациллин (PIPRIL) + ингибитор бета-лактамазы], азтреонам (AZACTAM) и некоторые цефалоспорины [цефтазидим (Fortum), цефепим (Maxipime)] и карбапенемы (ZIENAM) и др.) меропенем (Мерон),] достаточно эффективен. Хорошую активность также проявляют аминогликозиды [амикацин (БИКЛИН), гентамицин (Ребобацин и др.), Нетилмицин (ЦЕРТОМИЦИН), тобрамицин (ГЕРНЕБЦИН)] и фторхинолоны [(ципрофлоксацин (Cipro и др.), Левофлоксацин) (тавофлоксацин).
Согласно исследованию устойчивости Общества химиотерапии Пола Эрлиха в 2004 г. в каждом случае более 90% штаммов были чувствительны к меропенему и тобрамицину. Для амикацина, цефепима, цефтазидима, ципрофлоксацина и пиперациллина / тазобактама (тазобак) доля чувствительных штаммов варьировала от 75% до 80%.Однако следует отметить, что изоляты от пациентов в палатах общего профиля, обычно чувствительных к антибиотикам, были значительно более вероятными, чем изоляты в отделениях интенсивной терапии.
Лечение Pseudomonas Aeruginosa
Расчетное лечение инфекций, возбудителем которых является Pseudomonas aeruginosa, чтобы не отставать от местной резистентности. Для лечения опасных для жизни инфекций рассматриваются пиперациллин / тазобактам, цефтазидим, цефепим, имипенем или меропенем, обычно в сочетании с эффективными аминогликозидами Pseudomonas или фторхинолоном.Для менее тяжелых инфекций также может проводиться монотерапия бета-лактамным антибиотиком ципрофлоксацином или быть успешной, если адекватные дозы предотвращаются путем развития устойчивой субпопуляции. Лечение инфекций, вызываемых Pseudomonas, у больных муковисцидозом на основе антибиотикограммы. Если необходимо. Макролиды также связаны с их иммуномодулирующими свойствами для рассматриваемого лечения. Для начального лечения злокачественного наружного отита используется пиперациллин (12-20 г в день) в сочетании с тобрамицином (0.24 г в день) в течение четырех недель, а затем рекомендуется пероральный прием ципрофлоксацина (1–1,5 г в день) в течение нескольких месяцев.
|
Pseudomonas aeruginosa — microbewiki
Страница микробных биореалов по роду Pseudomonas aeruginosa
Классификация
Таксоны высшего порядка
| Домен | Бактерии |
|---|---|
| Тип | Протеобактерии |
| Класс | Гамма-протеобактерии |
| Заказать | Pseudomonadales |
| Семья | Псевдомонадные |
| Род | Псевдомонады |
| Группа пород | Группа синегнойной палочки |
Виды
| Род виды | Синегнойная палочка |
|---|
Описание и значение
Pseudomonas aeruginosa — это грамотрицательная палочковидная аспорогенная монофлагеллированная бактерия, обладающая невероятной универсальностью в питании.Это стержень длиной около 1-5 мкм и шириной 0,5-1,0 мкм. P. aeruginosa является облигатным респиратором, использующим аэробное дыхание (кислородом) в качестве оптимального метаболизма, хотя может также дышать анаэробно на нитратах или других альтернативных акцепторах электронов. P. aeruginosa может катаболизировать широкий спектр органических молекул, включая такие органические соединения, как бензоат. Таким образом, это делает P. aeruginosa очень распространенным микроорганизмом, поскольку он был обнаружен в таких средах, как почва, вода, люди, животные, растения, сточные воды и больницы (1).Во всех олиготропных водных экосистемах с высоким содержанием растворенного кислорода, но с низким содержанием питательных веществ для растений, преобладающим обитателем является P.aeruginosa , что явно делает его самым многочисленным организмом на Земле (2).
P.aeruginosa является условно-патогенным микроорганизмом человека. Он «условно-патогенный», потому что редко поражает здоровых людей. Вместо этого он часто колонизирует пациентов с ослабленным иммунитетом, например, больных муковисцидозом, раком или СПИДом (3). Это настолько мощный патоген, что, во-первых, он поражает две трети тяжелобольных госпитализированных пациентов, а это обычно предвещает более инвазивные заболевания.Во-вторых, P.aeruginosa является ведущим грамотрицательным условно-патогенным микроорганизмом в большинстве медицинских центров, смертность от которого составляет 40-60%. В-третьих, это осложняет 90% смертей от муковисцидоза; и, наконец, он всегда входит в тройку наиболее частых грамотрицательных патогенов и связан с наихудшими заболеваниями зрения (4). Кроме того, P.aeruginosa является очень важной почвенной бактерией, которая способна расщеплять полициклические ароматические углеводороды и производить рамнолипиды, хинолоны, цианистый водород, феназины и лектины (5).Он также проявляет внутреннюю резистентность к множеству различных типов химиотерапевтических агентов и антибиотиков, что делает его очень сложным для устранения патогеном (1).
P. aeruginosa впервые был описан как отдельный вид бактерий в конце XIX века, после разработки Пастером стерильных питательных сред. В 1882 году фармацевт Карл Гессар опубликовал первое научное исследование P. aeruginosa под названием «О сине-зеленой окраске бинтов».Это исследование показало характерную пигментацию P. aeruginosa: P. aeruginosa продуцирует водорастворимые пигменты, которые под воздействием ультрафиолета флуоресцируют сине-зеленым светом. Позже это было приписано пиоцианину, производному феназина, и это также отражало старые названия организма: Bacillus pyocyaneus , Bakterium aeruginosa , Pseudomonas polycolor и Pseudomonas pyocyaneus (3). P. aeruginosa имеет множество штаммов, включая штамм Pseudomonas aeruginosa PA01, Pseudomonas aeruginosa PA7, штамм Pseudomonas aeruginosa UCBPP-PA14 и штамм Pseudomonas aeruginosa 2192 (5).Большинство из них были выделены на основании характерного запаха аминоацетофенона, похожего на виноград, производства пиоцианина и структуры колоний на агаризованной среде (6).
Структура генома
P. aeruginosa имеет размер генома примерно от 5,2 до 7 миллионов пар оснований (Мбп) с 65% содержанием гуанина + цитозина. Это комбинация вариабельных дополнительных сегментов и консервативного ядра. Вариабельный вспомогательный геном характеризуется набором геномных островков и островков из первичного тРНК-интегрированного островного типа.Основной геном состоит из низкого уровня расхождения нуклеотидов 0,5% и консервативной синтении генов, что означает, что два или более гена, независимо от того, связаны они или нет, находятся на одной хромосоме (7).
P. aeruginosa имеет одинарную суперскрученную кольцевую хромосому в цитоплазме (4). Он также несет в себе множество мобилизующих хромосомы плазмид, которые очень важны для образа жизни организма как патоген. Плазмиды TEM, OXA и PSE, например, кодируются для продукции бета-лактамазы, которая необходима для ее устойчивости к антибиотикам, что позволяет обеспечить P.aeruginosa как грозный патоген (8).
Двумя штаммами, имеющими полную последовательность генома, являются Pseudomonas aeruginosa PA01 и Pseudomonas aeruginosa PA14 (9):
— В 2000 году группа добровольцев «ученых, занимающихся псевдомонадой», в том числе из Вашингтонской корпорации PathoGenesis Corportaion и Департамента биологии Калифорнийского университета в Сан-Диего, работала в рамках проекта аннотаций сообщества Pseudomonas aeruginosa (PseudoCAP) для публикации полная последовательность генома Pseudomonas aeruginosa PA01.Это было сделано потому, что знание геномной последовательности предоставит новую информацию об этой бактерии как патогене, а также об ее экологической универсальности и генетической сложности. Его бактериальный геном, насчитывающий 6264403 пары оснований, является крупнейшим из когда-либо секвенированных. Он также содержит 5 570 предсказанных открытых рамок считывания (ORF) и, таким образом, почти имеет генетическую сложность простых эукариот, таких как Saccharomyces cerevisiae . Используя полногеномный отбор проб, полный геном Pseudomonas aeruginosa PA01 в 6,3 Мбит / с очень похож на геном P.aeruginosa , за одним важным исключением, которое представляет собой инверсию примерно четверти генома Pseudomonas aeruginosa PA01. Эта инверсия происходит в результате гомологичной рекомбинации локусов рРНК и рРНК, и более ранние исследования инверсий геномных последовательностей локусов рибосомной ДНК в S. typhimurium и E. coli предполагают, что эта инверсия может иметь адаптивное значение (10).
— Полная последовательность генома Pseudomonas aeruginosa PA14 в настоящее время разрабатывается учеными Гарвардской медицинской школы.Целью данного исследования является получение общедоступных данных о геноме Pseudomonas aeruginosa PA14. Этап проекта по секвенированию с дробовиком был завершен в 2005 году, в результате было получено 6,54 Мбит / с последовательности PA14. В настоящее время его сравнивают с геномом Pseudomonas aeruginosa PA01, и предварительные результаты показали, что они очень похожи, но имеют несколько областей заметных различий, таких как вставка 107911bp в PA14, которая отсутствует в PA01. Примерно их 96.3% последовательности ДНК PAO1 находится в PA14, а 92,4% последовательности ДНК PA14 находится в PA01 (11).
Строение и метаболизм клеток
Белок F — поскольку P. aeruginosa является грамотрицательным микробом, он имеет внешнюю мембрану, которая содержит белок F (OprF). OprF действует как порин, позволяя определенным молекулам и ионам проникать в клетки, и как структурный белок, поддерживающий форму бактериальных клеток. Поскольку OprF обеспечивает внешнюю мембрану P. aeruginosa с пределом исключения 500 Да, он снижает проницаемость внешней мембраны, что является желательным свойством, поскольку он снижает поступление вредных веществ в клетку и дает P.aeruginosa обладает высокой устойчивостью к антибиотикам (12).
Flagellum and Pili — P. aeruginosa использует свой одиночный и полярный жгутик для передвижения и демонстрации хемотаксиса полезных молекул, таких как сахара. Его штаммы имеют жгутики либо a-типа, либо b-типа, эта классификация основана в первую очередь на размере и антигенности субъединицы флагеллина. Жгутик очень важен на ранних стадиях инфекции, поскольку он может прикрепляться к тканям хозяина и проникать в них (13).Как и его жгутик, пили P. aeruginosa в значительной степени способствуют его способности прикрепляться к поверхностям слизистых оболочек и эпителиальным клеткам. В частности, именно кончик пилей отвечает за прикрепление к поверхности клетки-хозяина. P. aeruginosa содержат N-метилфенилаланин (NMePhe) или пили IV типа (1). Пили представляют собой длинные полярные филаменты, состоящие из гомополимеров белка пилина, который кодируется геном pilA (4). В целом, жгутик и пили P. aeruginosa имеют сходные функциональные возможности (для прикрепления) и структуру (обе представляют собой нитчатые структуры на поверхности клетки), а их подвижность контролируется RpoN, особенно во время первоначального прикрепления к человеку-хозяину и ниже. условия с низким содержанием питательных веществ (1).
При заражении своего хозяина P. aeruginosa испытывает недостаток железа, поскольку депривация железа инфекционным патогеном является ключевой частью врожденного защитного механизма человека. Чтобы преодолеть эту проблему, P. aeruginosa синтезирует два сидерофоров: пиохелин и пиовердин. P. aeruginosa затем выделяет эти сидеофоры наружу клетки, где они прочно связываются с железом и возвращают железо в клетку. Кроме того, P. aeruginosa может также использовать железо из энтеробактина, специального сидерофора, производимого E.coli для транспорта железа, чтобы удовлетворить его потребность в железе (14).
P. aeruginosa — факультативный аэроб; его предпочтительный метаболизм — дыхание. Он получает энергию за счет передачи электронов от глюкозы, восстановленного субстрата, к кислороду, конечному акцептору электронов (15). Распад глюкозы требует, чтобы она окислилась до глюконата в периплазме, а затем она будет доставлена внутрь внутренней мембраны с помощью специальной энергозависимой системы захвата глюконата. Попав внутрь, глюконат фосфорилируется до 6-P-глюконата, который входит в центральный метаболизм для выработки энергии для клетки (16).Однако, когда P. aeruginosa находится в анаэробных условиях, P. aeruginosa использует нитрат в качестве концевого акцептора электронов (17). В условиях окислительного стресса P. aeruginosa синтезирует Fe- или Mn-содержащие ферменты супероксиддисмутазы (SOD), которые катализируют очень реактивную реакцию O- на h3O2 и O2. Он также детоксифицирует h3O2 до O2 и h3O с помощью каталазы (1).
Экология
Поскольку P. aeruginosa может жить как в неодушевленной, так и в человеческой среде, он был охарактеризован как «повсеместный» микроорганизм.Такая универсальность стала возможной благодаря большому количеству ферментов, которые позволяют P. aeruginosa использовать различные вещества в качестве питательных веществ. Наиболее впечатляюще то, что P. aeruginosa может переключаться с выращивания в немукоидной среде на слизистую, что сопровождается большим синтезом альгината. В неодушевленной среде P. aeruginosa обычно обнаруживается в водоемах, загрязненных животными и людьми, например в сточных водах и стоках внутри и за пределами больниц. Он также встречается в плавательных бассейнах и гидромассажных ваннах, потому что теплые температуры благоприятствуют его росту (3).Однако, поскольку он процветал в теплых условиях, было установлено, что он является виновником сыпи в горячей ванне, при которой прямой контакт между кожей и зараженной водой из ванны вызывает зуд инфицированной кожи и окрашивает ее в бугристый красный цвет ( 19). Кроме того, P. aeruginosa является условно-патогенным микроорганизмом человека, который вызывает хронические инфекции у пациентов с муковисцидозом и является основной причиной смерти от грамотрицательных бактерий (подробнее в разделе «Патология») (3).
Хотя большинство P.aeruginosa -растение вредно для растения, недавнее исследование обнаружило штамм P. aeruginosa , который фактически поддерживает рост растений. Эта характеристика, наряду с тем фактом, что P. aeruginosa может разлагать полициклические ароматические углеводороды, предполагает будущее использование P. aeruginosa для экологической детоксикации синтетических химикатов и пестицидов и в промышленных целях (3). Psuedomonas aeruginosa уникальна своей способностью заражать как людей, так и растения, это один из немногих организмов, способных заразить оба царства.
Группы P. aeruginosa имеют тенденцию образовывать биопленки, представляющие собой сложные бактериальные сообщества, которые прикрепляются к различным поверхностям, включая металлы, пластмассы, материалы для медицинских имплантатов и ткани. Биопленки характеризуются тем, что они «прикреплены для выживания», потому что, когда они сформированы, их очень трудно разрушить. В зависимости от местоположения биопленки могут быть как полезными, так и вредными для окружающей среды. Например, биопленки, обнаруженные на камнях и гальке под водой озер и прудов, являются важным источником пищи для многих водных организмов.Напротив, те, которые образовались внутри водопроводных труб, могут вызвать засорение и коррозию (19) (20).
Патология
P. aeruginosa редко вызывает заболевание у здоровых людей. Обычно это связано с пациентами, чья иммунная система нарушена из-за болезней или травм. Он получает доступ к тканям этих пациентов через ожоги, для пострадавших от ожогов или через основное заболевание, такое как кистозный фиброз. Во-первых, P. aeruginosa прикрепляется к тканевым поверхностям с помощью своего жгутика, пилей и экзо-S; затем он размножается, создавая заразную критическую массу; и, наконец, он повреждает ткани, используя факторы вирулентности (21).Поскольку мощные экзотоксины и эндотоксины, выделяемые P. aeruginosa во время бактериемии, продолжают инфицировать хозяина даже после того, как антибиотики убили P. aeruginosa , острые заболевания, вызываемые P. aeruginosa , имеют тенденцию быть хроническими и опасными для жизни. Более того, за исключением штамма кистозного фиброза, большинство штаммов P. aeruginosa, атакующих больных, не имеют слизистой оболочки (2). И даже несмотря на то, что у небольшого количества пациентов, инфицированных P. aeruginosa, развился тяжелый сепсис с поражениями с черными центрами, у большинства пациентов не было явных патологических эффектов колонизации (22).
Муковисцидоз (МВ) — наиболее распространенное аутосомно-рецессивное заболевание у кавказцев. При мутации хромосомы 7 легкое с МВ не может транспортировать хлорид (Cl-), натрий (Na +) и воду от базолатерального к секреторному эпителию. Это нарушение солевого и водного баланса в клетке приводит к образованию густой слизи, которая становится идеальным домом для потенциальных патогенов. P. aeruginosa атакует пациентов с МВ через дыхательные пути и, попав внутрь, использует свой жгутик для перехода в зону гипоксии, среду с низким содержанием кислорода.В этом месте P. aeruginosa претерпевает переход от аэробного микроба к анаэробному и начинает анаэробно формировать биопленки. Как только это сформировано, P. aeruginosa в этом сообществе могут ощущать свою популяцию через зондирование кворума, где они выделяют феромоны с низким молекулярным весом, которые позволяют им общаться друг с другом (23). Это дает им возможность противостоять многим защитным средствам, включая антибиотики против Pseudomonas, такие как тикарциллин, цефтазидим, тобрамицин и ципрофлоксацин, потому что, как только бактерии почувствуют, что их внешний слой биопленки разрушается, внутренние слои станут сильнее, чтобы восстановить сообщество (24). P. aeruginosa также устойчив ко многим антибиотикам и химиотерапевтическим средствам из-за их внутренней устойчивости. Это вызвано низкой проницаемостью внешней мембраны для антибиотиков и продуцированием β-лактамаз против множественных оттокных насосов и β-лактамных антибиотиков (22).
P. aeruginosa связывается с другими клетками посредством кворум-зондирования. Эта форма коммуникации позволяет клеткам регулировать выработку генов, что приводит к контролю определенных функций клетки.Одним из ферментов, отвечающих за восприятие кворума, является тирозинфосфатаза (TpbA). Этот фермент передает сигналы восприятия внеклеточного кворума продукции полисахаридов и образованию биопленок вне клеток (32). P. aeruginosa прикрепляется к поверхностям путем образования биопленок. Определение кворума может быть лекарственной мишенью для лечения инфекций, вызванных P. aeruginosa . Подавление кворума используется для блокировки сигнального механизма определения кворума и предотвращения образования биопленки у P.aeruginosa . И-Ху Донг и его коллеги смогли предотвратить образование биопленок у мышей в лабораторных условиях (33).
P. aeruginosa секретирует множество вирулентных факторов, колонизирующих клетки своего хозяина. Например, экзотоксин А, наиболее токсичный белок, продуцируемый P. aeruginosa , катализирует АДФ-рибозилирование с образованием АДФ-рибозил-EF-2, который ингибирует синтез белка в клетках-хозяевах. Более того, эластаза, внеклеточная протеаза цинка, атакует эукариотические белки, такие как коллаген и эластин, и разрушает структурные белки клетки.Он также расщепляет человеческий иммуноглобин и альфа-белки сыворотки (1).
Кроме того, P. aeruginosa заражает животных. В эксперименте мышам вводили внутривенную инъекцию вирулентного вируса P. aeruginosa , и эти животные обычно умирали в течение 24-48 часов. Когда вводилась меньшая доза, проявлялись характерные признаки инфекции, такие как потеря веса, очаговые поражения печени, селезенки и почек с последующей смертью в течение 3-10 дней. P. aeruginosa также вызывает вспышки пневмонии у морских свинок, и хотя он также поражает растения, в этой области проводилось не так много исследований (22).
Pseudomonas aeruginosa — это патогенный микроорганизм, широко распространенный в окружающей среде. Эпидермальные инфекции часто возникают в результате проникновения P. aeruginosa через первую линию защиты человека-хозяина и попадания в организм через кожу в месте открытой раны. P. aeruginosa является обычным членом больничных бактериальных сообществ, где он может инфицировать людей с ослабленным иммунитетом, включая жертв ожогов. P. aeruginosa является источником бактериемии у пострадавших от ожогов [36]. После серьезного повреждения кожи преобладание P.aeruginosa в окружающей среде увеличивает вероятность попадания организмов в кровоток через открытые глубокие эпидермальные ткани пострадавшего от ожога [36]. Предыдущие исследования опосредованной антителами защиты хозяина показали, что на пятый день после первоначального ожога экспрессия рецептора Fc снижается в полиморфно-ядерных лейкоцитах (PMN). Без рецептора Fc хемотаксис PMN значительно снижается, и PMN становятся менее эффективными в предотвращении инфекции [36].
P. aeruginosa может передаваться хозяину через фомитов, переносчиков и работников больниц, которые являются потенциальными носителями штаммов патогена с множественной устойчивостью к антибиотикам.Более того, любой P. aeruginosa, уже присутствующий на коже пострадавшего от ожога до травмы, может превратиться из безобидного организма на поверхности кожи в источник инфекции в кровотоке и тканях того же человека [36].
Пили и жгутики P. aeruginosa играют жизненно важную роль в инфицировании ожогов и ран [36]. Контролируемое инфицирование ожоговых ран на моделях животных и растений штаммами P. aeruginosa, лишенными пилей и жгутиков, демонстрирует тенденцию к снижению вирулентности.Без этих морфологических факторов вирулентности бактерии демонстрируют значительно сниженную выживаемость в месте раны и сниженную способность распространяться в организме хозяина [36]. Распространение P. aeruginosa в организме-хозяине также зависит от продукции микроорганизма эластазы и других механизмов протеазы. Бактериальная эластаза и другие бактериальные протеазы разрушают белки хозяина, в том числе структурные белки внутри мембран, разрушая физические барьеры хозяина против распространения инфекции.Эластаза также помогает P. aeruginosa избежать цитотоксичности, опосредованной фагоцитозными антителами, на участке раны, ингибируя хемотаксис моноцитов [36].
Идентификация:
Макроморфология (запах):
Крупные плоские колонии зеленоватого цвета (диаметром 2-4 мм) с неровными краями и типичным металлическим блеском. Цвет наиболее заметен, например, на TS-агаре. Иногда на кровяном агаре получается прозрачная зона гемолиза. Имеет характерный запах (карамельный, клубничный или малиновый).Некоторые штаммы продуцируют зеленый флуоресцентный пигмент пиовердин. Некоторые штаммы также могут производить синий пигмент, пиоцианин.
Микроморфология: Небольшой подвижный стержень (0,5-0,8 х 1,5-3 мкм) с монотриховым жгутиком.
Грамм -:
Рис. 65: 5. Окрашивание по грамму Pseudomonas aeruginosa, штамм ATCC 27853. Поле B представляет собой частичное увеличение (3 раза) A. Длина масштабной линейки соответствует 5 мкм. Дата: 24.03.2011. Г-
Метаболизм: часто классифицируется как аэробный, но может также использовать NO3- в качестве конечного акцептора электронов в дыхательной цепи.Следовательно, его следует классифицировать как факультативно анаэробный!
Каталаза / оксидаза: + / + Триптофаназа — Цитрат +, метиловый красный -, Фогес-Проскауэр -.
Спец. Char .: Оптимальная температура: 37 ° C, но может расти и при 42 ° C. Хозяева: крупный рогатый скот, собаки, лошади, норки, домашняя птица, овцы, рептилии и т. Д. (Включая людей). Резервуар: Окружающая среда: почва, вода и т. Д. Болезни (швед.): Мастит, пневмония, отит мм. Болезни (английский): мастит, пневмония, отит и т. Д.
Применение в биотехнологии
стр.aeruginosa , как и многие другие Pseudomonas, могут разлагать ароматические углеводороды, такие как метилбензолы, которые являются побочными продуктами нефтяной промышленности и обычно используются в качестве растворителей для эмалей и красок, а также при производстве лекарств и химикатов. Метилбензолы считаются загрязнителями окружающей среды, которые присутствуют в атмосфере, под землей и почвами, а также в поверхностных водах (25). P. aeruginosa может расщеплять толуол, простейшую форму метилбензола. P. aeruginosa разлагает толуол путем окисления метильной группы до альдегида, спирта и кислоты, которая затем превращается в катехол. Следовательно, P. aeruginosa может использоваться для борьбы с загрязнением (26).
Текущие исследования
Влияние космического полета на экспрессию микробных генов и вирулентность (микроб)
— Национальное управление по аэронавтике и исследованию космического пространства (НАСА) и Институт биодизайна при Университете штата Аризона в настоящее время проводят исследовательский проект под названием «Эксперимент с микробами».В этом эксперименте три микробных патогена Pseudomonas aeruginosa , Salmonella typhimurium и Candida albicans отправляются в космос, чтобы увидеть, как меняются их генетические реакции и вирулентность. Эти три микроба рассматривались как потенциальная угроза здоровью космонавтов, так как P. aeruginosa заразил водную систему космического корабля и заразил члена экипажа в эпоху Аполлона. Таким образом, понимание их адаптации и вирулентности в условиях микрогравитации даст ученым больше информации о космической среде экипажа и лучше подготовит космонавтов к будущим исследованиям космоса.Микробы были помещены в автономные культуральные камеры, и после приземления на землю одна треть образца будет использоваться для исследований вирулентности, а оставшаяся часть будет храниться замороженной при -80 ° C. Поскольку это текущий исследовательский проект, никаких результатов не было, но ученые НАСА очень надеются, что это исследование приведет к новым открытиям вакцин против этих микробов здесь, на Земле, и во время космического полета (27).
Комбинация ПЦР и серологии повышает диагностику колонизации / инфекции Pseudomonas aeruginosa при муковисцидозе
— Методы микробиологического культивирования часто используются для ранней диагностики P.aeruginosa у пациентов с муковисцидозом (МВ). Однако эти методы имеют некоторые недостатки, поскольку P. aeruginosa может быть не обнаружено, поскольку первоначальная инфекция обычно имеет низкую плотность. Затем было высказано предположение, что серология и полимеразная цепная реакция (ПЦР) могут быть лучшими методами обнаружения ранней стадии инфекции P. aeruginosa у детей с МВ на ранней стадии. Эксперимент проводился путем сбора мокроты и сыворотки у 87 детей с МВ, средний возраст 9 лет.7 лет. Потом, 1) ПЦР выполняли на мокроте, нацеленной на ген маннозодегидрогеназы P. aeruginosa algD GDP. 2) Серологическое исследование было выполнено против антигенов P. aeruginosa : экзотоксина А, эластазы и щелочной протеазы. 3) Была проведена комбинация ПЦР и серологии. Что касается результатов, то использование только метода ПЦР или серологии не дало статистически значимых отличий от методов микробиологического культивирования. Однако комбинация ПЦР и серологии выявила намного больше пациентов, чем любой из двух методов по отдельности.Следовательно, комбинированный метод, включающий ПЦР, будет точным методом для ранней диагностики колонизации P. aeruginosa у пациентов с МВ (28).
Геномный анализ показывает, что вирулентность Pseudomonas aeruginosa является комбинаторной.
— Сравнение между штаммом P. aeruginosa PA01 и более вирулентным P. aeruginosa PA14 было выполнено для идентификации новых генов вирулентности. Сначала было выполнено секвенирование генома «дробовика» на PA14 с использованием 65 800 плазмид с фрагментами ДНК PA14 размером 2–4 т.п.н.Затем был реализован метод на основе ПЦР с дальним диапазоном, чтобы определить, сходны ли определенные геномы P. aeruginosa с геномами PA01 или PA14. Было обнаружено, что хотя гемон PA14 (6,5 Мбит / с) несколько больше, чем у PA01 (6,3 Мбит / с), геномы PA14 и PA01 очень похожи. 58 кластеров генов из PA14 отсутствовали в PA01, и предполагалось, что некоторые из этих генов делают PA14 намного более вирулентным, чем PA01. Геномотипирование с помощью микрочипов 18 различных штаммов у C.elegans , однако, показала, что эти 58 кластеров генов PA14 не коррелировали с вирулентностью этих штаммов. Таким образом, был сделан вывод, что вирулентность у P. aeruginosa является как комбинаторной, так и многофакторной, и что гены, необходимые для того, чтобы один штамм был патогенным, не требовались для вирулентности в других штаммах (29).
УФ-световой тест флуоресцентного желто-зеленого пигмента в питательном бульоне
Исследования, также проведенные в микробиологической лаборатории Университета Лойола в Чикаго, показали, что Pseudomonas aeruginosa вырабатывает зеленовато-желтый флуоресцентный пигмент в питательном бульоне и при гидролизе казеина.После помещения этого флуоресцентного пигмента под УФ-свет мы наблюдали флуоресцентный сине-зеленый пигмент в пробирке. (35)
Рис. 6A Thr
При дефиците железа в результате действия пиовердинов образуется желтовато-зеленый флуоресцентный пигмент, термин, названный Турфрейджером для группы соединений, имеющих (1S) -5-амино-2,3- хромофор дигидро-8,9-дигидрокси-1H-пиримидо [1,2a] хинолин-1-карбоновой кислоты. На Фигуре 6А показаны различные типы групп пиовердина, которые могут быть получены на основе вариаций их пептидной цепи.Эти пигментные соединения растут только при ограничении содержания железа в среде для выращивания. На рис. 6А показаны три различные sv-подгруппы пиовердина P. aeruginosa . Поскольку эти три структуры пиовердина (также известные как ферри-пиовердины) не продуцируются никакими другими видами Pseudomonas , они могут быть быстрым способом идентификации конкретных бактерий, Pseudomonas aeruginos . (34)
Список литературы
1) Ледерберг, Джошуа и др. Псевдомонас .Энциклопедия микробиологии. Второе издание. Том 3. Сан-Диего, 2000. с. 876-891.
2) Костертон В. и Анвар H. Pseudomonas aeruginosa: микроб и патоген. Pseudomonas aeruginosa Инфекции и лечение. 1994. С. 1-17.
3) Ботценхардт К. и Доринг Г. Экология и эпидемиология Pseudomonas aeruginosa . Pseudomonas aeruginosa как оппортунистический патоген. 1993. стр. 1-7.
4) Фик Р. Pseudomonas aeruginosa — микробная гиена и ее роль в заболевании: введение. Pseudomonas aeruginosa : Оппортунист. 1993. стр. 1-6.
5) Сайт Национального центра биотехнологической информации
6) Джиларди, Г. Культурные и биохимические аспекты идентификации глюкозо-неферментирующих грамотрицательных палочек. Неферментирующиеся грамотрицательные палочки. 1985. С. 17-24.
7) Вильманн, Л., Вагнер, Г., Крамер *, Н., Зиберт, Б., Гудовиус, П., Моралес, Г., Ко, Т., Делден, К., Вайнель, К., Сликерс П. и Ту Б. «Популяционная структура Pseudomonas aeruginosa ».Preceedings of the National Academy of Sciences of the United States of America. 2007. Том 104. с. 8101–8106.
8) Крейг В. и Эберт С. Антимиробиологическая терапия Pseudomonas aeruginosa Инфекций. Pseudomonas aeruginosa Инфекции и лечение. 1994. стр. 470-491.
9) База данных генома Pseudomonas
10) Стовер, К., Фам, К., Эрвин, Л., Мизогучи, Д., Уорренер, П., Хики, Дж., Бринкман, Л., Хуфнагл, О., Ковалид, Д., М. .Лагроу, Р.Л. Гарбер, Л. Голтри, Э. Толентино, С. Вестброк-Вадман, Ю. Юань, Л.Л. Броуди *, С. Н. Колтер, Фолджер, Р., Кас, А., Ларбиг, К., Лим², Р., Smith², K., Spencer², D., Wong², K., Wu², Z., Paulsenk, J., Reizer, Z., Saier, H., Hancock³, R., Lory, S., и Olson, V. «Полная последовательность генома Pseudomonas aeruginosa PA01, условно-патогенного микроорганизма». Природа. 2000. Том 406. с. 961-964.
11) P. aeruginosa Проект геномного секвенирования PA14
12) Станисич В.и Ричмонд М. Перенос генов в роду Pseudomonas . Генетика и биохимия Pseudomonas . 1975. с. 170-175.
13) Делден, К. Факторы вирулентности в Pseudomonas aeruginosa . Псевдомонас . 2004. с. 1-7.
14) Кокс, С. Железо и вирулентность Pseudomonas aeruginosa . Pseudomonas aeruginosa : Оппортунист. 1993. стр. 41-45.
15) Rabaey, K. и Verstraete, W. «Микробные топливные элементы: новая биотехнология для производства энергии».ТЕНДЕНЦИИ в биотехнологии. 2005. Том 23.
16) Рохо Ф. и Динамарка А. Подавление катаболитов и физиологический контроль. Псевдомона с. 2004. с. 365-366.
17) Валлс, М., Кейз, И., и Лоренцо, В. Транскрипция, опосредованная rpoN-зависимыми промоторами. Псевдомонас . 2004. с. 398-302.
18) Центр по контролю и профилактике заболеваний
19) Центр биопленочной инженерии
20) Браун М. и Симит А. Противомикробные агенты и биопленки.Медицинское значение биопленок. 2003. с. 36-38.
21) Ирвин, Рэндалл. Прикрепление и колонизация Pseudomonas aerugionsa: роль поверхностных структур. ‘ Pseudomonas aeruginosa как оппортунистический патоген. 1993. стр. 19-36.
22) Лоубери, Э. Биологическое значение синегнойной палочки: медицинские аспекты. Генетика и биохимия псевдомонад. 1975. с. 37-43.
23) Холден М. и Уильямс П. «Анализ кворума». Энциклопедия наук о жизни.2001 г.
24) Смайли А. и Хассетт Д. Pseudomonas aeruginosa Инфекции биопленки при кистозном фиброзе. Биопленки, инфекции и антимикробная терапия. 2006. с. 155-158.
25) Пипер, Д., Штадлер-Фриче, К., Схоломан, М., и Кнакмасс, Х. Метаболизм 2-хлор-4-метилфеноксиацетата с помощью Alcaligenes eutrophus JMP 134: последствия для разложения хлор- и метила -Замещенные ароматические соединения через орто-расщепление. Pseudomonas Молекулярная биология и биотехнология.1992. стр. 268-272.
26) Джонсон, Г., Олсен, Р. «Множественные пути разложения толуола в Burkholderia sp. Штамм JS150 ». Прикладная и экологическая микробиология. 1997. Том 63. с. 4047-4052. [1]
27) Национальное управление по аэронавтике и исследованию космического пространства
28) Филхо, Л., Татено, А., Мартинс, К., Чернышев, А., Гарсия, Д., Хауг, М., Мейснер, К., Родригес, К., и До, Г. » Сочетание ПЦР и серологии увеличивает диагноз Pseudomonas aeruginosa Колонизация / инфекция при муковисцидозе.Детская пульмонология. 2007. Том 42. с. 938–944.
29) Ли, Д., Урбах, Дж., Ву, Г., Либерати, Н., Фейнбаум, Р., Мията, С., Диггинс, Л., Хе, Дж., Сосье, М., Дезиель , E., Friedman, L., Li, L., Grills, G., Montgomery, K., Kucherlapati, R., Rahme, L., and Ausubel, F. «Геномный анализ показывает, что Pseudomonas aeruginosa вирулентности. Комбинаторный ». Геномная биология. 2007. Том 7. [2]
30) Отредактировали студенты: Вивек Брахмбхатт и Варун Гарг из М. Глоговски в Университете Лойолы.http://web.ebscohost.com/ehost/pdfviewer/pdfviewer?vid=4&hid=104&sid=0029bc6b-e73c-4b8c-8882-42c0b9d6cedf%40sessionmgr112.
31) Мэлоун, Джейкоб Г., Тина Джагер и Кристиан Спенглер. «YfiBNR опосредует циклическое формирование и устойчивость малых колоний, зависимых от Cyclic Di-GMP, у Pseudomonas Aeruginosa». Патогены PLoS 7.3 (2010): 1-17. Премьера «Академический поиск». Интернет. 24 апреля 2010 г.
32) Uedal, A. & Wood, T.K. (2009). «Связь между восприятием кворума, c-di-GMP, полисахаридом pel и образованием биопленок у синегнойной палочки через тирозинфосфатазу TpbA (PA3885).»Публичная научная библиотека патогенов. Июнь 2009 г., том 5 (6).
33) Dong, Y.H., Wang, L.-H., & Zhang, L.-H. (2007). «Микробные инфекции, подавляющие кворум: механизмы и последствия». Философские труды Королевского общества B, 362 (1483), 1201-1211.
34) [1] Herbert. «Сидерофоры патогенных флуоресцентных псевдомонад человека». Текущие темы в медицинской химии 1.1 (2001): 1-6. Премьера «Академический поиск». Интернет. 27 апреля 2010 г.
35) Под редакцией студентов: Сафи Хан и Мишель Чуа из М. Глоговски из Университета Лойолы.http://web.ebscohost.com/ehost/pdfviewer/pdfviewer?vid=5&hid=119&sid=4ad96fae-039a-487e-8c86-3de5c67d301f%40sessionmgr104
36) Под редакцией студентов: Кэти Бейтс и Эшли Морс из М. Глоговски в Университете Лойолы. Lyczak, JB, Cannon, CL, Pier, GB. «Установление инфекции Pseudomonas aeruginosa: уроки разностороннего оппортуниста». Микробы и инфекции. 2000. Том 2. Выпуск 9. с. 1051-1060.
37) «ВетБакт». VetBact. N.p., n.d. Интернет.
38) Уокер, Трэвис С., Харш Пал Байс, Эрик Дезиель, Герберт П. Швейцер, Лоуренс Г. Раме, Рэй Фолл и Хорхе М. Виванко. «Взаимодействие Pseudomonas Aeruginosa с корнями растений. Патогенность, образование биопленок и экссудация корней». Физиология растений. Американское общество биологов растений, n.d. Интернет. 11 мая 2016.
Написано Челси Дао, ученицей Рэйчел Ларсен
Под редакцией KLB
Отредактировали студенты: Вивек Брамбхатт и Варун Гарг / Мишель Чуа и Сафи Хан из Мэри Глоговски из Университета Лойола, Ирина Рохас и Аарон Бегелин из Гамильтон-колледжа
.Pseudomonas aeruginosa
Pseudomonas — это род обычных бактерий, обитающих в почве и воде. Большинство видов безвредны, но некоторые являются условно-патогенными микроорганизмами, которые могут инфицировать животных, растения и людей. P. aeruginosa — это тип, который часто ассоциируется с болезнями человека.
ФАКТЫ: Pseudomonas — это род обычных бактерий, обитающих в почве и воде.Большинство видов безвредны, но некоторые являются условно-патогенными микроорганизмами, которые могут инфицировать животных, растения и людей. Pseudomonas aeruginosa — это тип, который часто ассоциируется с болезнями человека. В последние годы P. aeruginosa превратился в супербактерии, устойчивые к наиболее часто используемым антибиотикам. Наряду с MRSA и C. diff, P. aeruginosa адаптировалась к лекарствам, что сделало стандартные методы лечения инфекций гораздо менее эффективными. Всемирная организация здравоохранения даже оценила P. aeruginosa как одну из трех важнейших угроз в своем списке бактерий, наиболее нуждающихся в новых антибиотиках.
Супербактерии представляют собой огромную глобальную угрозу, вызывающую более 700 000 смертей в год. В США у 2 миллионов человек ежегодно развиваются инфекции, устойчивые к антибиотикам, и более 20 000 человек умирают. Неправильное и чрезмерное использование противомикробных препаратов у людей, животных и растений повысило устойчивость супербактерий. Сами врачи не могут устранить P. aeruginosa и другие супербактерии. Из-за взаимосвязи людей, животных и окружающей среды для победы над супербактериями потребуются совместные усилия ученых, ветеринаров, медицинских работников, политиков и общественности.
У здоровых людей P. aeruginosa может вызывать инфекции уха и глаз. Также может появиться кожная сыпь, особенно после воздействия плохо хлорированных горячих ванн и бассейнов. При заражении больными людьми с ослабленной иммунной системой P. aeruginosa может вызывать инфекции крови, пневмонию и другие тяжелые заболевания после операции. В больницах эти бактерии могут распространяться через руки медицинских работников или через зараженные катетеры, унитазы, инструменты и оборудование. P. aeruginosa чрезвычайно адаптивна и повсеместна.Этот стойкий микроб находится на подъеме, и его нельзя недооценивать как супербактерии.
.