Как разводить аламинол для дезинфекции инструментов
Фармакологическое действие Аламинола
Видео: Стерилизация и дезинфекция инструмента
Раствор Аламинол при проведении дезинфекции эффективен в отношении:
- Микобактерий туберкулеза;
- Грибов рода Кандида;
- Большинства бактерий, включая различных возбудителей внутрибольничных инфекций;
- Дерматофитов;
- Различных вирусов, включая энтеро-, полио-, ротавирусы, острые респираторные вирусные инфекции, ВИЧ-инфекции, герпес, возбудители парентеральных вирусных гепатитов.
Форма выпуска и состав Аламинола
В его состав входит глиоксаль и алкилдиметилбензиламмоний хлорида (ЧАС), а также краситель, поверхностно-активное вещество и вода.
Показания к применению Аламинола
- Дезинфекции изделий, которые используются в медицинских целях;
- Дезинфекции помещений, мебели, поверхностей, инвентаря, оборудования, салфеток, перевязочного материала, одноразового белья (перед утилизацией), различных предметов, используемых для ухода за пациентами;
- Предстерилизиационной очистки эндоскопов и инструментов, прилагающихся к ним.

Кроме того, регулярное применение Аламинола способствует предотвращению размножения плесневелых грибов в помещениях (жилых и нежилых).
Каких-либо противопоказаний к применению Аламинола по инструкции нет.
1% раствор Аламинола применяют для дезинфекции и предупреждения распространения инфекций бактериального происхождения (за исключением туберкулеза). Как правило, им протирают поверхности, санитарно-техническое оборудование, предметы ухода за пациентами (включая изделия из пластмассы, резины, стекла и металла).
5%, 8% и 10% растворы Аламинола по инструкции рекомендовано применять погружением в раствор для дезинфекции медицинского инвентаря при вирусных, бактериальных и грибковых заболеваниях, а также при туберкулезе и кандидозе. Также эти растворы используют в стоматологии — для обработки пластмассовых, стеклянных, инструментов, металлических предметов. Резиновые изделия обрабатывают 8% и 10% раствором средства.
Инструкцией определено, как разводить Аламинол для проведения различных видов дезинфекции.
Согласно инструкции, Аламинол в разведенном виде можно использовать многократно в течение 10 дней в случаях, если не изменился внешний вид (помутнение или изменение цвета).
При попадании на кожные покровы 1-10% раствор Аламинола может вызвать их раздражение и покраснение. В этом случае необходимо немедленно смыть средство с кожи, после чего обработать поверхность смягчающим кремом.
В случае попадания Аламинола в глаза, их следует промыть большим количеством воды, после чего закапать 1-2 капли 30% сульфацила натрия.
Условия и сроки хранения
Обзор дезинфицирующего средства Аламинол
Аламинол – это концентрированное дезинфицирующее средство, имеющее слабый запах и синий оттенок.
Это дезсредство повсеместно применяется для обработки поверхностей в медицинских учреждениях, общепите, салонах красоты и в местах пребывания детей.
В составе Аламинола отсутствует хлор. Он состоит из алкилдиметилбензиламмония хлорида и глиоксаля. Средство эффективно против бактерий (в том числе туберкулеза), вирусов, грибков «Candida». Хранить Аламинол следует в недоступном месте для предупреждения случайного отравления детей и животных.
Область применения Аламинола
- Область применения дезсредства широкая:
- Обработка инструментов перед стерилизацией;
- Проведение дезинфекции в помещениях, в которых оказываются услуги в сфере красоты и косметологии;
- Профилактика образования плесени;
- Обеззараживание в период распространения инфекций.
Преимущества использования Аламинола:
- Средство не представляет опасности для человека, при попадании на кожу легко смывается проточной водой (смазать Каппадермом или любым другим увлажняющим кремом).

- Эффективность средства лабораторно доказана (есть заключения государственных НИИ).
- Нейтральная реакция к нержавейке и высоколегированным медицинским сплавам, минимальное воздействует на металлы.
- Не оказывает фиксированного воздействия на слюну, кровь и другие органические соединения.
- Срок хранения раствора в закрытом виде до 10 дней. При появлении мутного осадка или взвесей его использовать нельзя.
- Дезинфекцию проводят двумя способами – протиранием или замачиванием.
- Доступная стоимость средства.
- Аламинол годен в течение года при условии хранения в темном месте при средних температурах в плотно закрытой емкости.
При случайном употреблении средства внутрь необходимо выпить много воды и принять активированный уголь в количестве 10-15 таблеток. К врачу обязательно нужно обратиться за помощью.
Для обработки маникюрных инструментов используется 5-8% раствор Аламинола. Работать со средством рекомендуется только в перчатках, с применением закрытых емкостей. Хранить Аламинол нужно отдельно от других препаратов.
Хранить Аламинол нужно отдельно от других препаратов.
Если обработка инструмента Аламинолом проводилась с нарушениями, это может привести к возникновению дефектов на поверхности металла. Таким инструментом пользоваться нельзя, его утилизируют.
Как разводить Аламинол?
Препарат производится в виде концентрата, перед использованием его необходимо разводить питьевой водой в специальной пластиковой емкости. Расчет пропорции составляющих достаточно простой: 1 литр готового 1% раствора содержит 10 мл Аламинола. Исходя из расчетов, чтобы получить 5% раствор потребуется 50 мл средства и т.д. Чтобы получить точную концентрацию, воды берут в объеме, недостающем до литра: к примеру, на 60 мл Аламинола следует брать 940 мл воды.
1-1,5% раствор средства применяют для обработки рабочего места с целью уничтожения бактерий. Препарат 3-5%-ной концентрации способен уничтожить вирусы, бактерии, в том числе и туберкулез. Более сильная концентрация раствора (8-10%) эффективно справляется с грибковыми инфекциями. Для определения дозировки концентрата рекомендуется использовать обычный медицинский одноразовый шприц (на другую порцию следует брать новый шприц).
Для определения дозировки концентрата рекомендуется использовать обычный медицинский одноразовый шприц (на другую порцию следует брать новый шприц).
Применение Аламинола для дезинфекции
Заводская инструкция по применению содержит полную информацию по дезинфицирующему препарату. Ее разрабатывали химики-технологи на основании проводимых испытаний в НИИ дезинфектологии России. Поэтому рекомендуется сохранять вкладыш весь период хранения средства и при необходимости уточнять особенности применения и работы с Аламинолом.
Дезраствор в процессе его использования в работе необходимо держать в емкостях, плотно закрытых. Контейнер должен быть изготовлен из материалов, химически нейтральных по отношению к другим веществам. Это может быть емкость из металла, покрытого эмалью, или пластиковая. Оптимальная температура для раствора – до 18 градусов.
Для защиты кожи рук от воздействия раствора Аламинола необходимо использовать перчатки из нитрила, резины либо силикона. В противном случае при открытом контакте рук с раствором приведет к появлению раздражения кожи. Чтобы очистить сложные места на инструменте, нужно окунуть его в раствор и обработать щеткой. Закрывающийся инструмент проходит обработку в раскрытом виде, например, это могут быть секаторы, ножницы хирургического и парикмахерского назначения, медицинские зажимы, кусачки. В медицинских учреждениях инструмент очищают сразу же, пока загрязнения свежие – это делается быстро и без особых усилий. Загрязнения, которые видны на поверхности, снимают салфеткой. А потом инструмент опускают в раствор. Спустя время использованные салфетки погружают в другой раствор, после утилизируют.
Чтобы очистить сложные места на инструменте, нужно окунуть его в раствор и обработать щеткой. Закрывающийся инструмент проходит обработку в раскрытом виде, например, это могут быть секаторы, ножницы хирургического и парикмахерского назначения, медицинские зажимы, кусачки. В медицинских учреждениях инструмент очищают сразу же, пока загрязнения свежие – это делается быстро и без особых усилий. Загрязнения, которые видны на поверхности, снимают салфеткой. А потом инструмент опускают в раствор. Спустя время использованные салфетки погружают в другой раствор, после утилизируют.
Аламинол — Ниопик — дезинфицирующее средство, 3л
НАЗНАЧЕНИЕ:
# дезинфекция поверхностей в помещениях, предметов обстановки, санитарно-технического оборудования, белья, предметов ухода за больными при инфекциях бактериальной (включая туберкулез), вирусной, грибковой (кандидозы, дерматофитии) этиологии
# дроведения генеральных уборок в ЛПУ, на объектах коммунальной службы, предприятиях общественного питания
# дезинфекция, в том числе совмещенной с предстерилизационной очисткой, изделий медицинского назначения (включая хирургические и стоматологические инструменты) и предстерилизационной очистки, не совмещенной с дезинфекцией, эндоскопов и инструментов к ним.
СОСТАВ:
действующие вещества: 5% алкилдиметилбензиламмоний хлорида (ЧАС) и 8% глиоксаля, а также поверхностно-активное вещество, краситель и вода.
СВОЙСТВА:
прозрачная жидкость ярко-синего цвета, имеет слабый запах отдушки, хорошо смешивается с водой. рН концентрата 3,5+0,8.
ФАСОВКА:
полиэтиленовые емкости вместимостью 1л и 3л.
МИКРОБИОЛОГИЯ:
эффективно в отношении бактерий (включая возбудителей внутрибольничных инфекций), микобактерий туберкулеза, грибов рода Кандида, дерматофитов, вирусов (полио-, энтеро-, ротавирусов, герпеса, возбудителей парентеральных вирусных гепатитов, ВИЧ-инфекции, острых респираторных вирусных инфекций).
ТОКСИЧНОСТЬ:
концентрат по параметрам острой токсичности по ГОСТ 12.1.007-76 относится к 3 классу умеренно опасных веществ при введении в желудок и к 4 классу малоопасных веществ при нанесении на кожу; оказывает выраженное местно-раздражающее действие на кожу и слизистые оболочки глаз, ингаляционно малоопасен в виде паров. Рабочие pacтворы проявляют слабое местно-раздражающее действие, не обладают сенсибилизирующими свойствами.
Рабочие pacтворы проявляют слабое местно-раздражающее действие, не обладают сенсибилизирующими свойствами.
ПРИМЕНЕНИЕ:
дезинфекцию растворами средства осуществляют способами погружения (изделия медицинского назначения, предметы ухода за больными, белье) и протирания (поверхности в помещениях, санитарно-техническое оборудование, предметы ухода за больными).
СРОК ГОДНОСТИ:
дезинфекцию растворами средства осуществляют способами погружения (изделия медицинского назначения, предметы ухода за больными, белье) и протирания (поверхности в помещениях, санитарно-техническое оборудование, предметы ухода за больными).
ВРЕМЕННОЕ НАСТАВЛЕНИЕ
по применению аламинола в ветеринарии для дезинфекции и снижения техногенного загрязнения (в порядке широкого производственного испытания в 2003-2005 гг.)
1. ОБЩИЕ ПОЛОЖЕНИЯ
1.1.Аламинол дезинфицирующее средство, содержащее в качестве действующих веществ глиоксаль (8,0%) и катамин АБ (5,0%), а также неонол
(15,0%) и краситель.
1.2. По внешнему виду препарат представляет собой прозрачную жидкость ярко-синего цвета со слабым специфическим запахом. В воде растворяется в любых соотношениях с обильным пенообразованием. Рабочие растворы аламинола не вызывают коррозии металлов, не портят
обрабатываемые материалы, обладают моющими свойствами.
1.3. Выпускают препарат расфасованным в полимерные канистры вместимостью 2-5 дм3, упакованные в ящики дощатые или из гофрированного картона. Масса одной упаковки не более 25 кг.
1.4. Каждую канистру маркируют согласно ТУ с указанием предприятия-изготовителя, названия препарата, назначения и способа применения, мер предосторожности, массы нетто, номера партии, даты изготовления, срока годности и номера ТУ и снабжают временным наставлением по применению препарата.
1.5. Аламинол хранят в таре завода-изготовителя в закрытых складскихпомещениях при температуре от 5 до 25°С. Гарантийный срок хранения присоблюдении условий хранения — 1 год со дня изготовления. Рабочие растворы аламинола сохраняют активность в течение 10 дней.
1.6. Аламинол транспортируют всеми видами транспорта в условиях, обеспечивающих сохранность продукта и тары в соответствии с правилами перевозки грузов, действующих на данном виде транспорта.
2. БИОЛОГИЧЕСКИЕ СВОЙСТВА
2.1.Препарат аламинол обладает широким спектром действия в отношении бактерий (исключая споровые формы), вирусов и грибов и
обезвреживает сырье животного происхождения от техногенных загрязнителей (радионуклидов).
2.2. По параметрам острой токсичности аламинол относится к III классу умеренно опасных веществ при введении в желудок (LD50 3925 +180 мг/кг) и к IV классу малоопасных веществ при нанесении на кожу (LD50 2500 мг/кг). Ингаляционно малоопасен. Обладает слабой сенсибилизацией, оказывает выраженное местно-раздражающее действие на кожу и слизистые оболочки.
Рабочие растворы обладают слабым местно-раздражающим действием и не вызывают сенсибилизации.
2.3. Наличие на обеззараживаемой поверхности органических загрязнений снижает дезинфекционную активность препарата, в связи с чем при подготовке объектов к дезинфекции необходимо проводить их тщательную механическую очистку.
2.4.При обработке аламинолом сырья животного происхождения его качество не снижается.
3. ПОРЯДОК ПРИМЕНЕНИЯ ПРЕПАРАТА
3.1. Аламинол применяют для проведения:
— профилактической дезинфекции производственных, бытовых и вспомогательных помещений и оборудования в животноводческих (птицеводческих, звероводческих) хозяйствах, питомниках, вивариях, зоопарках, ветеринарных клиниках и лечебницах, спецодежды работников животноводства, автомобильного транспорта, используемого для перевозки животных и сырья животного происхождения;
— вынужденной дезинфекции перечисленных выше объектов при инфекционных болезнях животных (птицы) бактериальной и вирусной
этиологии, при которых действующей инструкцией — предусмотрен контроль качества дезинфекции по выделению бактерий группы кишечной палочки и стафилококков;
— дезинфекции всех видов немытой трепаной шерсти, неблагополучной по бактериальным и вирусным инфекциям, на фабриках первичной обработки шерсти;
— обезвреживания всех видов немытой трепаной шерсти от техногенных загрязнителей с одновременной ее дезинфекцией при бактериальных и вирусных инфекциях;
-дезинфекции пушно-мехового сырья (шкурки норки, песца, лисиц), неблагополучного по бактериальным, вирусным ннфекциям и дерматомикозам. а также в качестве антисептика в процессе промышленной переработки шкурок, полученных от клинически здоровых зверей.
а также в качестве антисептика в процессе промышленной переработки шкурок, полученных от клинически здоровых зверей.
3.2.Препарат применяют в отсутствии животных (птицы) методом орошения, а также в виде механических или термомеханических аэрозолей.
Для получения аэрозолей используют установку «Аист-2», генераторы аэрозолей АГ-УД-2, АГ-Л6, САГ, ЦАГ и др. в соответствии с инструкцией по их применению.
3.3. Для дезинфекции методом орошения на объектах, перечисленных в п.
З.1., применяют 5%-ные растворы аламинола при норме расхода 0,25-0,3 л/м2.
Экспозиция 3 ч.
Дезинфекцию помещений инкубаториев и технологического оборудования (инкубационные и выводные шкафы) проводят путем орошения 2%-ным раствором аламинола из расчета 0,25-0,3 л/м2. Экспозиция 3 ч.
Во всех случаях при обработке методом орошения элементов из пористых материалов (неокрашенное дерево, цемент, резина) норму расхода препарата увеличивают до 0,3-0,5 л/м2, раствор наносят дробно в два приема с интервалом в 15-20 мин.
3.4. Для аэрозольной дезинфекции закрытых помещений с
профилактической целью, а также вынужденной дезинфекции приинфекционных боле бактериальной и вирусной этиологии, при которых
качество дезинфекции контролируют по выделению бактерий группы кишечнойпалочки стафилококков, применяют 5%-ные растворы аламинола из расчета 20 мл/м3 внутреннего объема помещений. Экспозиция дезинфекции в инкубаториях 2 ч, а при обработке помещений для содержания животных (птицы) — 24 ч.
3.5. Для текущей дезинфекции при туберкулезе применяют 5%-ные растворы аламинола, двукратно с интервалом 1 ч по 0,3-0,5 л/м2 на каждое
орошение. Общая экспозиция — 12 ч.
3.6. По окончании дезинфекции поилки, кормушки, каналы навозоудаления, другие поверхности помещений и оборудования, с которыми
контактируют животные (птица), обмывают водой, помещения проветривают и просушивают. С остальных поверхностей смывание остатков препарата не требуется.
3.7.Спецодежду обеззараживают методом погружения в 5%-ный раствор аламинола (4 л на 1 кг).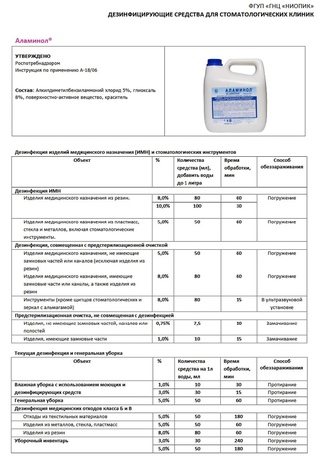 Экспозиция дезинфекции при бактериальных
Экспозиция дезинфекции при бактериальных
инфекциях 1 ч; при вирусных, грибковых инфекциях и туберкулезе — 3 ч.
По окончании экспозиции спецодежду ополаскивают водой с последующей стиркой в обычном порядке.
3.8. Допускается применение аламинола для дезинфекции методоморошения отдельных свободных от животных станкомест в занятых
животноводческих помещениях.
3.9. Аламинол применяют для проведения дезинфекции всех видов немытой трепаной шерсти, неблагополучной по бактериальным и вирусным инфекциям, на фабриках первичной обработки Шерсти путем погружения ее на
30 мин в раствор аламинола нужной концентрации, начальная температура которого составляет 48-500С при жидкостном коэффициенте 30.
3.9.1. Для обеззараживания шерсти, полученной из хозяйств неблагополучных по инфекционным болезням бактериальной и вирусной этиологии:
— тонкой, полутонкой, кроссбредной, цигайской, применяют 1% растворы, температура которых составляет 49-500 С. Экспозиция обеззараживания 30 мин при жидкостном коэффициенте (отношении массы раствора к массе шерсти) 30.
— полугрубой и грубой — 0,75% растворы при вышеприведенных режимах.
3.10. Для дезактивации радионуклидов и одновременной дезинфекции всех видов немытой трепаной шерсти используют препарат по режимам, указанным в п.п. 3.9.1., обрабатывая шерсть отдельными партиями с уровнем радиационного загрязнения до 3,0 мР/час.
По окончании экспозиции шерсть направляют на дальнейшую мойку по типовому технологическому режиму с максимальным противотоком моющего раствора и исключением из технологического процесса промышленной сортировки.
Моечные растворы при последующей чистке моечных машин после переработки вышеуказанной шерсти не перекачиваются, а сбрасываются полностью в очистные сооружения.
3.11. Дезинфекцию и обеззараживание пушно-мехового сырья (шкурки норки, песца, лисиц) в процессе его промышленной переработки проводят путем погружения на 16-20 ч в отмочный раствор, используя для сырья из хозяйств неблагополучных по бактериальным инфекциям 1% раствор, вирусным инфекциями — 0,75%, дерматомикозам — 1,5%; для сырья из благополучных хозяйств — 0,1% раствор.
Начальная температура раствора составляет 33-35°С при жидкостном коэффициенте 10 (шкурки норки) и 25 (шкурки песцов и лисиц).
По окончании экспозиции (отмоки) шкурки направляются на дальнейшую переработку в соответствии с действующей Единой технологией переработки.
4. КОНТРОЛЬ КАЧЕСТВА ДЕЗИНФЕКЦИИ И ДЕЗАКТИВАЦИИ
4.1. Качество дезинфекции контролируют в соответствии с методикой,изложенн в инструкции «Проведение ветеринарной дезинфекции объектов животноводства» (1988 г.).
В качестве нейтрализатора используют 0,1-0,5%-ные растворы мыла или стерильную воду.
4.2.Режимы дезинфекции пушно-мехового сырья при дерматомикозах разработаны применительно к возбудителям трихофитии и микроспории
пушных зверей.
4.3.Для проведения контроля качества дезактивации шерсти от кип мытой шерсти с однотипными по радиоактивной загрязненности показателямиотбирают пробы массой по 1,5 кг и помещают в упаковки из мешковины размером 50x20x10 см. Мытая шерсть с остаточной радиоактивностью выше ДУ (допустимых уровней) при необходимости может быть подвергнута повторной мойке в чистых моющих растворах и повторному дозиметрическому контролю.
4.3.1. Для определения радиоактивной загрязненности шерсти в кипах или упаковках массой по 1,5 кг датчик дозиметра перемещают на расстоянии 0,5-1,5 см от обследуемой поверхности. По наибольшему отклонению стрелки прибора снимают показания, а для руна шерсти — дозиметр в защите помещают в середину руна и производят измерение.
4.3.2. Уровни радиоактивного загрязнения мытой шерсти регламентированы документом «О порядке радиационного контроля за
пищевым сырьем и продовольственными товарами» № 12-24/1041 от 01.07.92 г., согласно которому содержание цезия-137 в шерсти не должно превышать 600 Бк/кг; рекомендациями Госсаннадзора СССР № 129-ДСП/167-9 от 14.10.86 г., по которым остаточная радиоактивность мытой шерсти по мощности экспозиционной дозы гамма-излучения — 25 мР/ч над естественным фоном от упаковок шерсти массой 1,5 кг размером 50x20x10 см, определенная прибором СРП-68-01.
5. МЕРЫ ЛИЧНОЙ БЕЗОПАСНОСТИ
5.1. Аламинол — малоопасное средство, однако при приготовлении и применении рабочих растворов следует избегать его попадания на кожу и в глаза. По окончании работы лицо и руки необходимо вымыть с мылом.
По окончании работы лицо и руки необходимо вымыть с мылом.
5.2. При проведении дезинфекции методом орошения необходимо использовать средства защиты: респираторы (РУ-60М или РПГ-67 с патроном марки А), защитные очки (ПО-2, ПО-3), резиновые перчатки, фартук.
5.3. При проведении аэрозольной дезинфекции используют аппараты, не требующие присутствия оператора в обрабатываемом помещении (Аист-2, АГ- УД-2, АГ-Л6, ЦАГ, САГ и др.).
5.4. При попадании препарата в глаза или на кожу — промыть их водой, а при попадании в желудок — промыть его большим количеством воды.
5.5. Работа с шерстью, загрязненной радионуклидами, регламентируется действующими нормами радиационной безопасности (НРБ-99) и основными санитарными правилами ОСП-72/87.
Временное наставление разработано ВНИИВСГЭ.
Одобрено секцией «Радиобиология» отделения ветеринарной медицины РАСХН (протокол № 2 от 01.11.2000 г.)
Одобрено Советом по ветеринарным препаратам Департамента ветеринарии Минсельхоза РФ, протокол № 5 от 13. 12.2000 г.
12.2000 г.
№ 001237-ОП
Аламинол инструкция по применению
АЛАМИНОЛ ИНСТРУКЦИЯ № А-18/06.
По применению средства “Аламинол” (ФГУП ”ГНЦ «НИОПИК”, Россия) для дезинфекции и
предстерилизационной очистки. Средство «Аламинол» является совместной разработкой
Государственного научного центра Федерального Государственного Унитарного Предприятия
“НИОПИК” и Федерального Государственного Учреждения Науки Научно-исследовательского
института дезинфектологии (НИИД) Роспотребнадзора.
Инструкция разработана НИИД.
Авторы: Цвирова И.М., Пантелеева Л.Г., Абрамова И.М., Белова А.С., Дьяков В.В., Федорова Л.С.,
Панкратова Г.П., Рысина Т.З., Закова И.М.
1. ОБЩИЕ СВЕДЕНИЯ.
1.1. Средство «Аламинол» представляет собой прозрачный жидкий концентрат от синего до
зелено-синего цвета, имеет слабый запах отдушки, хорошо смешивается с водой. В качестве
действующих веществ в состав средства входят 5% алкилдиметилбензиламмоний хлорида
(ЧАС) и 8% глиоксаля, а также поверхностно-активное вещество, краситель и вода;
рН концентрата 3,8+1,2.
Средство расфасовано в полиэтиленовые емкости вместимостью от 1 до 5 дм3.
Срок годности концентрата в невскрытой упаковке производителя при комнатной температуре
составляет 1 год.
Срок годности 1 — 10% рабочих растворов составляет 10 суток при условии их хранения в
закрытых емкостях в темном прохладном месте.
1.2. Средство обладает бактерицидными, туберкулоцидными, вирулицидными, фунгицидными,
а также моющими свойствами.
1.3. Средство (концентрат) по параметрам острой токсичности по ГОСТ 12.1.007-76 относится
к 3 классу умеренно опасных веществ при введении в желудок и к 4 классу малоопасных веществ
при нанесении на кожу; оказывает выраженное местно-раздражающее действие на кожу и
слизистые оболочки глаз, ингаляционно малоопасен в виде паров.
Рабочие pacтворы проявляют слабое местно-раздражающее действие, не обладают
сенсибилизирующими свойствами. ПДК алкилдиметилбензиламмоний хлорида в воздухе рабочей
ПДК алкилдиметилбензиламмоний хлорида в воздухе рабочей
зоны — 1,0 мг/м3 (аэрозоль, 2 класс опасности), глиоксаля — 2 мг/м3 с пометкой
«Требуется защита кожи и глаз».
1.4. Средство аламинол предназначено для:
— дезинфекции поверхностей в помещениях, предметов обстановки, санитарно-технического
оборудования, уборочного инвентаря, белья, предметов ухода за больными, медицинских отходов
(перевязочный материал, салфетки, белье однократного использования и т.п.; изделия медицинского
назначения однократного применения) перед их утилизацией при инфекциях бактериальной
(включая туберкулез), вирусной, грибковой (кандидозы, дерматофитии) этиологии; для проведения
генеральных уборок в ЛПУ, на объектах коммунальной службы, предприятиях общественного питания;
— для борьбы с плесневыми грибами;
— дезинфекции, в том числе совмещенной с предстерилизационной очисткой, изделий медицинского
назначения (включая хирургические и стоматологические инструменты) и предстерилизационной
очистки, не совмещенной с дезинфекцией, эндоскопов и инструментов к ним ручным способом;
— для предстерилизационной очистки, совмещенной и не совмещенной с дезинфекцией, изделий
из металлов (включая хирургические и стоматологические инструменты) механизированным
способом в ультразвуковых установках «Кристалл-5», «УЗВ-10/150-ТН-«РЭЛТЕК», «УЗО1/01-МЕДЭЛ»
и «УЗО3/01-МЕДЭЛ».
2. ПРИГОТОВЛЕНИЕ РАБОЧИХ РАСТВОРОВ.
Рабочие растворы средства готовят в стеклянных, эмалированных (без повреждения эмали),
пластмассовых емкостях путем добавления соответствующих количеств концентрата средства
к питьевой воде.
Таблица 7.
Режимы дезинфекции изделий медицинского назначения растворами средства “Аламинол”
при вирусных, бактериальных (включая туберкулез) и грибковых (кандидозы, дерматофитии)
инфекциях.
|
|
|
|
|
|
|
|
|
|
|
|
|
30-60 |
|
5. МЕРЫ ПРЕДОСТОРОЖНОСТИ.
5.1. При приготовлении рабочих растворов средства следует избегать его попадания на кожу
и в глаза.
5.2. Все работы со средством необходимо проводить с защитой кожи рук резиновыми перчатками.
5.3. Емкости, содержащие растворы средства, в которых проводят дезинфекцию объектов способом
погружения, держать закрытыми.
5.4. При работе со средством следует соблюдать правила личной гигиены. После работы лицо
и руки вымыть с мылом.
5.5. Средство следует хранить отдельно от лекарственных препаратов в местах, недоступных детям.
6. МЕРЫ ПЕРВОЙ ПОМОЩИ ПРИ СЛУЧАЙНОМ ОТРАВЛЕНИИ.
6.1. При случайном попадании средства в желудок необходимо выпить несколько стаканов воды,
с 10-20 измельченными таблетками активированного угля. При необходимости обратиться к врачу.
6.2. При попадании средства на кожу обильно промыть пораженное место водой, затем смазать
смягчающим кремом.
6.3. При попадании средства в глаза немедленно промыть их под проточной водой в течение
10-15 мин, затем закапать 1-2 капли 30% раствора сульфацила натрия. Обратиться к врачу.
8. УСЛОВИЯ ХРАНЕНИЯ, ТРАНСПОРТИРОВАНИЯ, УПАКОВКА.
8.1. Средство следует хранить в упаковке изготовителя в крытом вентилируемом складском
помещении при температуре от 0ОC до плюс 35ОС, отдельно от лекарственных препаратов,
пищевых продуктов, в местах, недоступных детям.
Средство замерзает при температуре минус 5ОС. После размораживания сохраняет свои свойства.
8.2. Средство транспортируют всеми видами транспорта при температуре от минус 20ОС до плюс
35ОС в соответствии с правилами перевозки грузов, действующими на этих видах транспорта,
в крытых транспортных средствах и условиях, обеспечивающих сохранность средства и упаковки.
8.3. Средство разливают в бутылки или канистры из полимерных материалов вместимостью от 1 до 5 дм3.
8.4. При случайной утечке средства его следует разбавить большим количеством воды или адсорбировать
впитывающими веществами (песок, опилки, ветошь, силикагель) и направить на утилизацию. Слив
Слив
растворов в канализационную систему допускается проводить только в разбавленном виде. При уборке
разлившегося средства использовать спецодежду, резиновый фартук, резиновые сапоги и средства
индивидуальной защиты — кожи рук (резиновые перчатки), глаз (защитные очки), органов дыхания
(универсальные респираторы типа РУ 60 М, РПГ-67 с патроном марки В). Попадание средства в
поверхностные/сточные воды не допускается.
СРЕДСТВО ДЛЯ ДЕЗИНФЕКЦИИ АЛАМИНОЛ
Аламинол — универсальное средство для дезинфекции и пред стерилизационной очистки, с широким антимикробным спектром действия. Страна-производитель: Россия Средство «Аламинол» представляет собой прозрачный жидкий концентрат от синего до зелено-синего цвета, имеет слабый запах отдушки, хорошо смешивается с водой. В качестве действующих веществ в состав средства входят 5% алкилдиметилбензиламмоний хлорида (ЧАС) и 8% глиоксаля, а также поверхностно-активное вещество, краситель и вода; рН концентрата 3,8+1,2. Срок годности концентрата в невскрытой упаковке производителя при комнатной температуре составляет 1 год. Срок годности 1 ― 10% рабочих растворов составляет 10 суток при условии их хранения в закрытых емкостях в темном прохладном месте. Средство обладает бактерицидными, туберкулоцидными, вирулицидными, фунгицидными, а также моющими свойствами. Средство (концентрат) по параметрам острой токсичности по ГОСТ 12.1.007-76 относится к 3 классу умеренно опасных веществ при введении в желудок и к 4 классу малоопасных веществ при нанесении на кожу; оказывает выраженное местно-раздражающее действие на кожу и слизистые оболочки глаз, ингаляционно малоопасен в виде паров. Рабочие pacтворы проявляют слабое местно-раздражающее действие, не обладают сенсибилизирующими свойствами. Средство предназначено для: — дезинфекции поверхностей в помещениях, предметов обстановки, санитарно-технического оборудования, уборочного инвентаря, белья, предметов ухода за больными, медицинских отходов (перевязочный материал, салфетки, белье однократного использования и т.
Срок годности концентрата в невскрытой упаковке производителя при комнатной температуре составляет 1 год. Срок годности 1 ― 10% рабочих растворов составляет 10 суток при условии их хранения в закрытых емкостях в темном прохладном месте. Средство обладает бактерицидными, туберкулоцидными, вирулицидными, фунгицидными, а также моющими свойствами. Средство (концентрат) по параметрам острой токсичности по ГОСТ 12.1.007-76 относится к 3 классу умеренно опасных веществ при введении в желудок и к 4 классу малоопасных веществ при нанесении на кожу; оказывает выраженное местно-раздражающее действие на кожу и слизистые оболочки глаз, ингаляционно малоопасен в виде паров. Рабочие pacтворы проявляют слабое местно-раздражающее действие, не обладают сенсибилизирующими свойствами. Средство предназначено для: — дезинфекции поверхностей в помещениях, предметов обстановки, санитарно-технического оборудования, уборочного инвентаря, белья, предметов ухода за больными, медицинских отходов (перевязочный материал, салфетки, белье однократного использования и т. п.; изделия медицинского назначения однократного применения) перед их утилизацией при инфекциях бактериальной (включая туберкулез), вирусной, грибковой (кандидозы, дерматофитии) этиологии; для проведения генеральных уборок в ЛПУ, на объектах коммунальной службы, предприятиях общественного питания; — для борьбы с плесневыми грибами; — дезинфекции, в том числе совмещенной с предстерилизационной очисткой, изделий медицинского назначения (включая хирургические и стоматологические инструменты) и предстерилизационной очистки, не совмещенной с дезинфекцией, эндоскопов и инструментов к ним ручным способом; — для предстерилизационной очистки, совмещенной и не совмещенной с дезинфекцией, изделий из металлов (включая хирургические и стоматологические инструменты) механизированным способом в ультразвуковых установках «Кристалл-5», «УЗВ-10/150-ТН-«РЭЛТЕК», «УЗО1/01-МЕДЭЛ» и «УЗО3/01-МЕДЭЛ». ПРИГОТОВЛЕНИЕ РАБОЧИХ РАСТВОРОВ. Рабочие растворы средства готовят в стеклянных, эмалированных (без повреждения эмали), пластмассовых емкостях путем добавления соответствующих количеств концентрата средства к питьевой воде (табл.
п.; изделия медицинского назначения однократного применения) перед их утилизацией при инфекциях бактериальной (включая туберкулез), вирусной, грибковой (кандидозы, дерматофитии) этиологии; для проведения генеральных уборок в ЛПУ, на объектах коммунальной службы, предприятиях общественного питания; — для борьбы с плесневыми грибами; — дезинфекции, в том числе совмещенной с предстерилизационной очисткой, изделий медицинского назначения (включая хирургические и стоматологические инструменты) и предстерилизационной очистки, не совмещенной с дезинфекцией, эндоскопов и инструментов к ним ручным способом; — для предстерилизационной очистки, совмещенной и не совмещенной с дезинфекцией, изделий из металлов (включая хирургические и стоматологические инструменты) механизированным способом в ультразвуковых установках «Кристалл-5», «УЗВ-10/150-ТН-«РЭЛТЕК», «УЗО1/01-МЕДЭЛ» и «УЗО3/01-МЕДЭЛ». ПРИГОТОВЛЕНИЕ РАБОЧИХ РАСТВОРОВ. Рабочие растворы средства готовят в стеклянных, эмалированных (без повреждения эмали), пластмассовых емкостях путем добавления соответствующих количеств концентрата средства к питьевой воде (табл. 1). Рабочие растворы средства «Аламинол» применяют: — для дезинфекции поверхностей в помещениях (пол, стены, жесткая мебель, приборы, оборудование), предметов ухода за больными (подкладные клеенки, грелки и т.д.), санитарно-технического оборудования (раковины, унитазы, ванны и др.), уборочного инвентаря, белья медицинских отходов (перевязочный материал, марлевые салфетки, халаты и т.п., изделия медицинского назначения однократного применения) по режимам, указанным в табл. 2-6; — для дезинфекции, в том числе совмещенной с предстерилизационной очисткой, изделий медицинского назначения (включая хирургические и стоматологические инструменты) из различных материалов (металлы, резины на основе натурального и силиконового каучука, пластмассы, стекло) и предстерилизационной очистки, не совмещенной с дезинфекцией, эндоскопов и инструментов к ним ручным способом по режимам, указанным в табл. 7-10; — для предстерилизационной очистки, совмещенной и не совмещенной с дезинфекцией, изделий из металлов (включая хирургические и стоматологические инструменты) механизированным способом в ультразвуковых установках «Кристалл-5», «УЗВ-10/150-ТН-«РЭЛТЕК», «УЗО1/01-МЕДЭЛ» и «УЗО3/01-МЕДЭЛ» в табл.
1). Рабочие растворы средства «Аламинол» применяют: — для дезинфекции поверхностей в помещениях (пол, стены, жесткая мебель, приборы, оборудование), предметов ухода за больными (подкладные клеенки, грелки и т.д.), санитарно-технического оборудования (раковины, унитазы, ванны и др.), уборочного инвентаря, белья медицинских отходов (перевязочный материал, марлевые салфетки, халаты и т.п., изделия медицинского назначения однократного применения) по режимам, указанным в табл. 2-6; — для дезинфекции, в том числе совмещенной с предстерилизационной очисткой, изделий медицинского назначения (включая хирургические и стоматологические инструменты) из различных материалов (металлы, резины на основе натурального и силиконового каучука, пластмассы, стекло) и предстерилизационной очистки, не совмещенной с дезинфекцией, эндоскопов и инструментов к ним ручным способом по режимам, указанным в табл. 7-10; — для предстерилизационной очистки, совмещенной и не совмещенной с дезинфекцией, изделий из металлов (включая хирургические и стоматологические инструменты) механизированным способом в ультразвуковых установках «Кристалл-5», «УЗВ-10/150-ТН-«РЭЛТЕК», «УЗО1/01-МЕДЭЛ» и «УЗО3/01-МЕДЭЛ» в табл. 11-14. Поверхности в помещениях протирают ветошью, смоченной раствором средства. Норма расхода рабочего раствора средства составляет 150 мл на 1 м кв. обрабатываемой поверхности. Санитарно-техническое оборудование обрабатывают с помощью щетки, ерша или протирают ветошью, смоченной в растворе средства. Норма расхода рабочего раствора ― 200 мл на 1 м кв. обрабатываемой поверхности оборудования. Белье замачивают в рабочем растворе средства из расчета 5 л раствора на 1 кг белья. По окончании дезинфекции бельё тщательно прополаскивают. Уборочный инвентарь погружают в раствор средства. По окончании дезинфекционной выдержки прополаскивают водой. Предметы ухода за больными полностью погружают в емкость с раствором средства или протирают ветошью, смоченной раствором средства. По окончании дезинфекции предметы ухода за больными тщательно промывают водой. Медицинские отходы из текстильных материалов (ватные тампоны, использованный перевязочный материал, одноразовое нательное и постельное белье, одежда персонала, маски и пр.
11-14. Поверхности в помещениях протирают ветошью, смоченной раствором средства. Норма расхода рабочего раствора средства составляет 150 мл на 1 м кв. обрабатываемой поверхности. Санитарно-техническое оборудование обрабатывают с помощью щетки, ерша или протирают ветошью, смоченной в растворе средства. Норма расхода рабочего раствора ― 200 мл на 1 м кв. обрабатываемой поверхности оборудования. Белье замачивают в рабочем растворе средства из расчета 5 л раствора на 1 кг белья. По окончании дезинфекции бельё тщательно прополаскивают. Уборочный инвентарь погружают в раствор средства. По окончании дезинфекционной выдержки прополаскивают водой. Предметы ухода за больными полностью погружают в емкость с раствором средства или протирают ветошью, смоченной раствором средства. По окончании дезинфекции предметы ухода за больными тщательно промывают водой. Медицинские отходы из текстильных материалов (ватные тампоны, использованный перевязочный материал, одноразовое нательное и постельное белье, одежда персонала, маски и пр. ) замачивают в 5% растворе средства в течение 3-х часов, затем утилизируют. Изделия медицинского назначения однократного применения из металлов, стекла, пластмасс погружают в 5,0% раствор средства на 60 мин, из резин – в 8,0% раствор на 60 мин, по окончании дезинфекции утилизируют. Для борьбы с плесенью поверхности в помещениях сначала очищают от плесени с помощью щетки или других приспособлений, затем двукратно с интервалом 15 мин или трехкратно обрабатывают 8,0% раствором средства. Время дезинфекционной выдержки при двукратной обработке составляет 3 часа, при трехкратной – 2 часа. Генеральные уборки в хирургических, акушерских, гинекологических, соматических стационарах, процедурных кабинетах, клинических, диагностических лабораториях, станциях переливания крови, ЛПУ стоматологического профиля проводят по режимам, рекомендованным для дезинфекции объектов при вирусных инфекциях; в противотуберкулезных и кожно-венерологических стационарах ― по режимам для соответствующих инфекций. При проведении профилактической дезинфекции и генеральных уборок на предприятиях общественного питания, коммунальных объектах (общежития, гостиницы и пр.
) замачивают в 5% растворе средства в течение 3-х часов, затем утилизируют. Изделия медицинского назначения однократного применения из металлов, стекла, пластмасс погружают в 5,0% раствор средства на 60 мин, из резин – в 8,0% раствор на 60 мин, по окончании дезинфекции утилизируют. Для борьбы с плесенью поверхности в помещениях сначала очищают от плесени с помощью щетки или других приспособлений, затем двукратно с интервалом 15 мин или трехкратно обрабатывают 8,0% раствором средства. Время дезинфекционной выдержки при двукратной обработке составляет 3 часа, при трехкратной – 2 часа. Генеральные уборки в хирургических, акушерских, гинекологических, соматических стационарах, процедурных кабинетах, клинических, диагностических лабораториях, станциях переливания крови, ЛПУ стоматологического профиля проводят по режимам, рекомендованным для дезинфекции объектов при вирусных инфекциях; в противотуберкулезных и кожно-венерологических стационарах ― по режимам для соответствующих инфекций. При проведении профилактической дезинфекции и генеральных уборок на предприятиях общественного питания, коммунальных объектах (общежития, гостиницы и пр. ), детских учреждениях средство используют в режимах, рекомендованных для дезинфекции при бактериальных инфекциях. Дезинфекцию, в том числе совмещенную с предстерилизационной очисткой, изделий ручным способом проводят в пластмассовых или эмалированных (без повреждения эмали) емкостях, закрывающихся крышками. Разъемные изделия погружают в раствор в разобранном виде. Изделия, имеющие замковые части, погружают раскрытыми, предварительно сделав ими в растворе несколько рабочих движений для лучшего проникновения раствора в труднодоступные участки изделий. Во время замачивания (дезинфекционной выдержки) каналы и полости должны быть заполнены (без воздушных пробок) раствором. Толщина слоя раствора над изделиями должна быть не менее 1 см. После окончания обработки изделия извлекают из емкости с раствором и отмывают их от остатков рабочего раствора средства в течение 3 мин проточной питьевой водой, с тщательным промыванием всех каналов. Очистку эндоскопов и инструментов к ним проводят с учетом требований санитарно-эпидемиологических правил СП 3.
), детских учреждениях средство используют в режимах, рекомендованных для дезинфекции при бактериальных инфекциях. Дезинфекцию, в том числе совмещенную с предстерилизационной очисткой, изделий ручным способом проводят в пластмассовых или эмалированных (без повреждения эмали) емкостях, закрывающихся крышками. Разъемные изделия погружают в раствор в разобранном виде. Изделия, имеющие замковые части, погружают раскрытыми, предварительно сделав ими в растворе несколько рабочих движений для лучшего проникновения раствора в труднодоступные участки изделий. Во время замачивания (дезинфекционной выдержки) каналы и полости должны быть заполнены (без воздушных пробок) раствором. Толщина слоя раствора над изделиями должна быть не менее 1 см. После окончания обработки изделия извлекают из емкости с раствором и отмывают их от остатков рабочего раствора средства в течение 3 мин проточной питьевой водой, с тщательным промыванием всех каналов. Очистку эндоскопов и инструментов к ним проводят с учетом требований санитарно-эпидемиологических правил СП 3. 1.1275-03 «Профилактика инфекционных заболеваний при эндоскопических манипуляциях» и методических указаний «Очистка, дезинфекция и стерилизация эндоскопов и инструментов к ним» (МУ 3.5.1937-04 от 04.03.2004г.). Растворы средства для предстерилизационной очистки изделий, в том числе совмещенной с их дезинфекцией, ручным способом могут быть использованы многократно в течение срока годности, если их внешний вид не изменился. При появлении первых признаков изменения внешнего вида (изменение цвета, помутнение раствора и т.п.) раствор необходимо заменить до истечения указанного срока. Во избежание разбавления растворов средства при многократном их использовании изделия следует погружать в раствор только после удаления с них влаги. Растворы средства для дезинфекции, совмещенной с предстерилизационной очисткой, инструментов механизированным способом в установках «Кристалл-5» и «УЗВ-10/150-ТН-«РЭЛТЕК» используют однократно. Инструменты размещают в корзине ультразвуковой установки не более чем в два слоя, таким образом, чтобы обеспечивался свободный доступ раствора к ним.
1.1275-03 «Профилактика инфекционных заболеваний при эндоскопических манипуляциях» и методических указаний «Очистка, дезинфекция и стерилизация эндоскопов и инструментов к ним» (МУ 3.5.1937-04 от 04.03.2004г.). Растворы средства для предстерилизационной очистки изделий, в том числе совмещенной с их дезинфекцией, ручным способом могут быть использованы многократно в течение срока годности, если их внешний вид не изменился. При появлении первых признаков изменения внешнего вида (изменение цвета, помутнение раствора и т.п.) раствор необходимо заменить до истечения указанного срока. Во избежание разбавления растворов средства при многократном их использовании изделия следует погружать в раствор только после удаления с них влаги. Растворы средства для дезинфекции, совмещенной с предстерилизационной очисткой, инструментов механизированным способом в установках «Кристалл-5» и «УЗВ-10/150-ТН-«РЭЛТЕК» используют однократно. Инструменты размещают в корзине ультразвуковой установки не более чем в два слоя, таким образом, чтобы обеспечивался свободный доступ раствора к ним. Мелкие стоматологические инструменты (боры, дрильборы и т.п.) укладывают в один слой в крышку чашки Петри, которую устанавливают в корзину ультразвуковой установки (крышку чашки Петри заполняют раствором средства). Контроль качества предстерилизационной очистки на наличие остаточных количеств крови проводят путем постановки азопирамовой или амидопириновой пробы согласно методикам, изложенным в методических указаниях «Контроль качества предстерилизационной очистки изделий медицинского назначения с помощью реактива азопирам (№ 28-6/13 от 28.05.88г.) и в «Методических указаниях по предстерилизационной очистке изделий медицинского назначения» (№ 28-6/13 от 08.06.82г.). Контролю подлежит 1% одновременно обработанных изделий одного наименования (но не менее трех изделий). УСЛОВИЯ ХРАНЕНИЯ, ТРАНСПОРТИРОВАНИЯ, УПАКОВКА Средство следует хранить в упаковке изготовителя в крытом вентилируемом складском помещении при температуре от 0ОC до плюс 35ОС, отдельно от лекарственных препаратов, пищевых продуктов, в местах, недоступных детям.
Мелкие стоматологические инструменты (боры, дрильборы и т.п.) укладывают в один слой в крышку чашки Петри, которую устанавливают в корзину ультразвуковой установки (крышку чашки Петри заполняют раствором средства). Контроль качества предстерилизационной очистки на наличие остаточных количеств крови проводят путем постановки азопирамовой или амидопириновой пробы согласно методикам, изложенным в методических указаниях «Контроль качества предстерилизационной очистки изделий медицинского назначения с помощью реактива азопирам (№ 28-6/13 от 28.05.88г.) и в «Методических указаниях по предстерилизационной очистке изделий медицинского назначения» (№ 28-6/13 от 08.06.82г.). Контролю подлежит 1% одновременно обработанных изделий одного наименования (но не менее трех изделий). УСЛОВИЯ ХРАНЕНИЯ, ТРАНСПОРТИРОВАНИЯ, УПАКОВКА Средство следует хранить в упаковке изготовителя в крытом вентилируемом складском помещении при температуре от 0ОC до плюс 35ОС, отдельно от лекарственных препаратов, пищевых продуктов, в местах, недоступных детям. Средство замерзает при температуре минус 5ОС. После размораживания сохраняет свои свойства. Средство транспортируют всеми видами транспорта при температуре от минус 20ОС до плюс 35ОС в соответствии с правилами перевозки грузов, действующими на этих видах транспорта, в крытых транспортных средствах и условиях, обеспечивающих сохранность средства и упаковки. Средство разливают в бутылки или канистры из полимерных материалов вместимостью от 1 до 5 дм3. При случайной утечке средства его следует разбавить большим количеством воды или адсорбировать впитывающими веществами (песок, опилки, ветошь, силикагель) и направить на утилизацию. Слив растворов в канализационную систему допускается проводить только в разбавленном виде. При уборке разлившегося средства использовать спецодежду, резиновый фартук, резиновые сапоги и средства индивидуальной защиты ― кожи рук (резиновые перчатки), глаз (защитные очки), органов дыхания (универсальные респираторы типа РУ 60 М, РПГ-67 с патроном марки В). Попадание средства в поверхностные/сточные воды не допускается.
Средство замерзает при температуре минус 5ОС. После размораживания сохраняет свои свойства. Средство транспортируют всеми видами транспорта при температуре от минус 20ОС до плюс 35ОС в соответствии с правилами перевозки грузов, действующими на этих видах транспорта, в крытых транспортных средствах и условиях, обеспечивающих сохранность средства и упаковки. Средство разливают в бутылки или канистры из полимерных материалов вместимостью от 1 до 5 дм3. При случайной утечке средства его следует разбавить большим количеством воды или адсорбировать впитывающими веществами (песок, опилки, ветошь, силикагель) и направить на утилизацию. Слив растворов в канализационную систему допускается проводить только в разбавленном виде. При уборке разлившегося средства использовать спецодежду, резиновый фартук, резиновые сапоги и средства индивидуальной защиты ― кожи рук (резиновые перчатки), глаз (защитные очки), органов дыхания (универсальные респираторы типа РУ 60 М, РПГ-67 с патроном марки В). Попадание средства в поверхностные/сточные воды не допускается.
Моющее средство бактерицидное «Аламинол»: инструкция по применению.
.Средство «Аламинол» инструкция по применению характеризует как концентрат, обладающий моющими, вирулицидными, бактерицидными и фунгицидными свойствами. Кроме того, этот препарат обладает выраженным туберкулоцидным действием, а также проявляет легкое местно-раздражающее действие. По параметрам токсичности раствор «Аламинол» относится к третьей категории так называемых умеренно опасных веществ при попадании в желудок и к четвертой категории малоопасных веществ при нанесении на кожу.Следует отметить, что концентрат препарата, разбавленный питьевой водой, не обладает сенсибилизирующими свойствами и проявляет слабое местно-раздражающее действие. Кроме того, такие дезинфицирующие средства (в том числе «Аламинол») не вдыхают в виде паров.
Особенности состава и формы выпуска
Выпускается антисептический препарат, действующий как на вирусы, так и на бактерии и грибки в виде жидкого концентрированного вещества.![]() Прозрачный раствор средства «Аламинол» (инструкция по применению это подтверждает) имеет слабый специфический запах и ярко-синий цвет.Что касается состава этого дезинфицирующего средства с широким спектром применения, в качестве активных ингредиентов используются 8% глиоксаля и 5% хлорида алкилдиметилбензиламмония. Комбинация этих двух веществ может эффективно подавлять активность грибков, таких как Candida, бактерии ВИЧ-инфекции, парентерального гепатита, туберкулезных микобактерий, герпеса и острых форм респираторных инфекций. В роли вспомогательных компонентов выступают вода и специальный краситель.
Прозрачный раствор средства «Аламинол» (инструкция по применению это подтверждает) имеет слабый специфический запах и ярко-синий цвет.Что касается состава этого дезинфицирующего средства с широким спектром применения, в качестве активных ингредиентов используются 8% глиоксаля и 5% хлорида алкилдиметилбензиламмония. Комбинация этих двух веществ может эффективно подавлять активность грибков, таких как Candida, бактерии ВИЧ-инфекции, парентерального гепатита, туберкулезных микобактерий, герпеса и острых форм респираторных инфекций. В роли вспомогательных компонентов выступают вода и специальный краситель.
Область применения концентрата
Используйте вирилицид «Аламинол», рекомендованный инструкцией по применению, в первую очередь, с целью дезинфекции различной мебели, поверхностей и помещений.Например, его можно разбавить водой для предстерилизационной очистки эндоскопов, инструментов и повязок. Для дезинфекции специального сантехнического оборудования и предметов ухода за больными инфекционными заболеваниями грибковой, бактериальной и вирусной этиологии отлично подходит препарат «Аламинол». Инструкция по применению рекомендует применять его в поликлиниках, в организациях общественного питания (например, в кафе и столовых), в учреждениях бытового обслуживания. В этом случае процедуру дезинфекции следует проводить как можно чаще.Это связано с тем, что при частом применении этого раствора снижается риск появления плесневых грибков в нежилых и жилых помещениях.
Инструкция по применению рекомендует применять его в поликлиниках, в организациях общественного питания (например, в кафе и столовых), в учреждениях бытового обслуживания. В этом случае процедуру дезинфекции следует проводить как можно чаще.Это связано с тем, что при частом применении этого раствора снижается риск появления плесневых грибков в нежилых и жилых помещениях.
Меры предосторожности
Используя «Аламинол», необходимо всегда соблюдать элементарные правила безопасности и обязательно использовать такие средства защиты, как резиновые перчатки. Даже небольшое количество рабочего раствора на коже может вызвать раздражение и покраснение кожи. По окончании всех необходимых процедур рекомендуется тщательно вымыть руки с моющим средством и обработать смягчающим лосьоном или кремом.
Мета-анализ рандомизированных контролируемых исследований
Эффективность дополнительного использования адъювантов для подготовки кишечника все еще неясна. В этом исследовании сравнивали 1 л полиэтиленгликоля плюс аскорбиновая кислота с режимами адъювантных препаратов (1 л ПЭГ-АА, меньший объем) с 2 л полиэтиленгликоля плюс аскорбиновая кислота (2 л ПЭГ-А, низкий объем), чтобы оценить, можно ли использовать адъюванты для снижения стандарта. дозировка слабительного дальше. В базе данных PubMed / MEDLINE, EMBASE, Cochrane Library и Web of Science был проведен поиск рандомизированных контролируемых испытаний (РКИ).Первичным результатом была эффективность подготовки кишечника, а вторичными результатами — переносимость пациентами и частота осложнений. Общее качество доказательств оценивалось с помощью инструмента разработки рекомендаций GRADEpro. Были включены пять РКИ с участием 1013 пациентов из Кореи. Большинство пациентов были амбулаторно из разных больниц. Объединенные данные не показали существенной разницы в частоте адекватной подготовки кишечника (89,3% против 89,4%, ОР 1, 95% ДИ 0,95–1,05), а также в частоте осложнений (ОР для тошноты 1.22, 95% ДИ 0,89–1,65,; ОР вздутия живота 0,96, 95% ДИ 0,73–1,28,; ОР для рвоты 0,69, 95% ДИ 0,32–1,50,; ОР боли в животе 1,01, 95% ДИ 0,61–1,69,). Но значительно более высокая степень готовности наблюдалась в меньшем объеме (85,1% против 67,9%, ОР 1,25, 95% ДИ 1,14–1,38). Качество доказательств первичного исхода было умеренным.
дозировка слабительного дальше. В базе данных PubMed / MEDLINE, EMBASE, Cochrane Library и Web of Science был проведен поиск рандомизированных контролируемых испытаний (РКИ).Первичным результатом была эффективность подготовки кишечника, а вторичными результатами — переносимость пациентами и частота осложнений. Общее качество доказательств оценивалось с помощью инструмента разработки рекомендаций GRADEpro. Были включены пять РКИ с участием 1013 пациентов из Кореи. Большинство пациентов были амбулаторно из разных больниц. Объединенные данные не показали существенной разницы в частоте адекватной подготовки кишечника (89,3% против 89,4%, ОР 1, 95% ДИ 0,95–1,05), а также в частоте осложнений (ОР для тошноты 1.22, 95% ДИ 0,89–1,65,; ОР вздутия живота 0,96, 95% ДИ 0,73–1,28,; ОР для рвоты 0,69, 95% ДИ 0,32–1,50,; ОР боли в животе 1,01, 95% ДИ 0,61–1,69,). Но значительно более высокая степень готовности наблюдалась в меньшем объеме (85,1% против 67,9%, ОР 1,25, 95% ДИ 1,14–1,38). Качество доказательств первичного исхода было умеренным. Результаты этого метаанализа показали, что 1 л PEG-AA может быть жизнеспособной альтернативой 2L PEG-A со сравнимой эффективностью, лучшими предпочтениями пациентов и отсутствием статистически значимых нежелательных явлений.
Результаты этого метаанализа показали, что 1 л PEG-AA может быть жизнеспособной альтернативой 2L PEG-A со сравнимой эффективностью, лучшими предпочтениями пациентов и отсутствием статистически значимых нежелательных явлений.
1. Введение
Колоноскопия имеет важное клиническое значение в профилактике колоректального рака [1]. Подчеркивается важность качества подготовки кишечника, поскольку это один из семи ключевых показателей эффективности, рекомендованных для колоноскопии Комитетом по качеству Европейского общества эндоскопии желудочно-кишечного тракта (ESGE) [2]. Однако до колоноскопии пациентов в основном беспокоила сама колоноскопия; страх перед колоноскопией сопровождался подготовкой кишечника [3, 4].
Существуют различные коммерчески доступные средства подготовки кишечника для его очищения. Кроме того, руководящие принципы рекомендуют препараты на основе полиэтиленгликоля (ПЭГ) в больших или малых объемах, а также препараты, не содержащие ПЭГ; они требуют клинической проверки для рутинной подготовки кишечника [5]. Принимая во внимание, что из-за более низкой стоимости схемы на основе 2-4 л ПЭГ являются предпочтительным методом и широко используются с момента появления раствора ПЭГ в 1980 году [6]. Объем раствора препарата считается основной проблемой переносимости и приемлемости пациентов, готовящихся к колоноскопии [7].
Принимая во внимание, что из-за более низкой стоимости схемы на основе 2-4 л ПЭГ являются предпочтительным методом и широко используются с момента появления раствора ПЭГ в 1980 году [6]. Объем раствора препарата считается основной проблемой переносимости и приемлемости пациентов, готовящихся к колоноскопии [7].
Вопросы плохой комплаентности и объема низкой переносимости слабительных средств при подготовке кишечника уже были рассмотрены. Уменьшение объема ПЭГ в методе 2 л ПЭГ плюс аскорбиновая кислота (ПЭГ-Asc) является безопасным и эффективным методом подготовки кишечника по сравнению с традиционным методом 4 л ПЭГ [8, 9]. В результате метод 2L PEG-Asc теперь рассматривается как действительная альтернатива стандартному PEG и одобрен Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США [10]. Однако дозировка этого режима все еще велика для приема внутрь.Кроме того, показано, что с предварительно упакованной диетой с низким содержанием остатков режим 1 л PEG-Asc не уступает раствору в небольшом объеме с точки зрения очищающей эффективности [11]. Для общей подготовки кишечника, хотя адъюванты, за исключением симетикона, не рекомендуются для рутинного использования [5, 12, 13], несколько недавних исследований в Корее показали, что дополнительное использование вспомогательного вещества вместе с традиционными средствами подготовки кишечника может уменьшить требуемый объем. .
Для общей подготовки кишечника, хотя адъюванты, за исключением симетикона, не рекомендуются для рутинного использования [5, 12, 13], несколько недавних исследований в Корее показали, что дополнительное использование вспомогательного вещества вместе с традиционными средствами подготовки кишечника может уменьшить требуемый объем. .
В текущем обзоре сравнивается эффективность 1 л ПЭГ с аскорбиновой кислотой плюс дополнительные лекарственные препараты (1 л ПЭГ-АА, меньший объем) с 2 л ПЭГ с режимами аскорбиновой кислоты (2 л ПЭГ-А, низкий объем) с использованием метааналитических методов.Это исследование направлено на изучение возможности использования дополнительных препаратов для PEG-Asc для снижения дозировки слабительного у большего числа пациентов.
2. Методы
2.1. Источники данных и стратегия поиска
Систематический поиск был выполнен двумя независимыми рецензентами (Синь Юань и Чжисинь Чжан) через PubMed / MEDLINE, EMBASE, Кокрановскую библиотеку и Web of Science (до 10 марта 2020 г. ) с предварительно определенными условиями поиска. Стратегия поиска (пример EMBASE в таблице S1) была сформулирована в соответствии с заголовком / входом медицинских предметов вместе с ключевыми словами, относящимися к «колоноскопия», «полиэтиленгликоль» и «1L.”Были включены только полные тексты, опубликованные на английском языке.
) с предварительно определенными условиями поиска. Стратегия поиска (пример EMBASE в таблице S1) была сформулирована в соответствии с заголовком / входом медицинских предметов вместе с ключевыми словами, относящимися к «колоноскопия», «полиэтиленгликоль» и «1L.”Были включены только полные тексты, опубликованные на английском языке.
После удаления повторяющихся исследований с помощью встроенной функции в программе EndNote были проверены заголовки и аннотации, а затем полные тексты потенциально релевантных исследований были проверены на соответствие критериям. Чтобы избежать упущения в литературе, мы также просмотрели ссылки на каждую литературу.
2.2. Критерии приемлемости исследования
Исследования были признаны подходящими согласно критериям PICOS: (1) участники (P): все взрослые, которым была сделана колоноскопия; (2) вмешательства (I) и сравнения (C): сравнение 1 л PEG-AA с 2 л PEG-A перед колоноскопией; (3) результат (O): первичный результат включает эффективность подготовки кишечника, измеренную по Бостонской шкале подготовки кишечника (BBPS), а вторичные результаты включают переносимость и осложнения, связанные с режимом; и (4) исследование (S): рандомизированные контролируемые испытания (РКИ).
2.3. Синтез данных
Основные характеристики (такие как возраст, пол, сопутствующие заболевания, показания к колоноскопии и меры по подготовке кишечника), показатели качества (общее время обследования, частота выявления аденомы (ADR), количество опытных эндоскопистов, частота интубации слепой кишки ( CIR)), а исходы (такие как частота адекватной подготовки кишечника (АД), общий балл и баллы по сегментам BBPS, переносимость и осложнения) были извлечены из соответствующих статей двумя независимыми исследователями (Xin Yuan и Lu Xu).Исходные наборы данных представлены в таблице S2. Любые разногласия между следователями разрешались арбитражем и разрешались путем взаимного обсуждения, и достигалось соглашение с помощью старшего следователя (Лэй Сюй).
2.4. Риск систематической ошибки и оценка достоверности
Качество исследования оценивалось с использованием инструмента Cochrane Collaboration для оценки риска систематической ошибки для РКИ. Инструмент включал семь областей оценки (таких как генерация случайной последовательности, сокрытие распределения, слепота участников и персонала, слепая оценка результатов, неполные данные, выборочная отчетность и другие систематические ошибки) и классифицируются как низкий, неясный или высокий риск. Из-за включения ограниченных исследований систематическая ошибка публикации оценивалась не с помощью воронкообразной диаграммы, а с помощью теста Эггера. Достоверность исследования оценивалась одним из авторов (Вейхонг Ван) с использованием подхода GRADEpro GDT (https: // gdt. Http://gradepro.org/app) для обобщения качества доказательств.
Из-за включения ограниченных исследований систематическая ошибка публикации оценивалась не с помощью воронкообразной диаграммы, а с помощью теста Эггера. Достоверность исследования оценивалась одним из авторов (Вейхонг Ван) с использованием подхода GRADEpro GDT (https: // gdt. Http://gradepro.org/app) для обобщения качества доказательств.
2,5. Статистический анализ
Извлеченные данные были последовательно собраны во всех подходящих исследованиях, объединены и сведены в таблицу в едином формате в Microsoft Excel.Статистический анализ проводился с использованием программного обеспечения RevMan (Review Manager, версия 5.3) и программного обеспечения STATA (StataMP, версия 14). Поскольку наш метаанализ включал переменные непрерывности, то есть оценку BBPS и дихотомические переменные, то есть готовность к повторению, они были отдельно рассчитаны и отображены с использованием лесных участков с фиксированной или случайной моделью эффектов. Для дихотомических событий был рассчитан относительный риск (ОР) вместе с 95% доверительным интервалом (ДИ). Поскольку включенные исходы были непрерывными переменными, объединенные оценки были рассчитаны как средние различия (MD), а также 95% доверительный интервал.Статистическая неоднородность испытаний оценивалась по критерию несогласованности и значению, которое было значимым, если было> 50% или. Если статистически значимо, то анализ исключения исследования проводился, когда наблюдались возможные источники клинической гетерогенности определенного исследования, и применялась модель случайных эффектов. Кроме того, при необходимости проводился анализ подгрупп.
Поскольку включенные исходы были непрерывными переменными, объединенные оценки были рассчитаны как средние различия (MD), а также 95% доверительный интервал.Статистическая неоднородность испытаний оценивалась по критерию несогласованности и значению, которое было значимым, если было> 50% или. Если статистически значимо, то анализ исключения исследования проводился, когда наблюдались возможные источники клинической гетерогенности определенного исследования, и применялась модель случайных эффектов. Кроме того, при необходимости проводился анализ подгрупп.
3. Результаты
3.1. Результаты поиска
Первоначальное исследование литературы дало 306 статей, 147 из которых были немедленно исключены из-за дублирования.Затем, после обзора названий и аннотаций, в общей сложности 135 исследований были отклонены, потому что они были либо неколоноскопическими исследованиями, либо отсутствием полных текстов, либо не сравнивали рассматриваемые препараты кишечника. После этого 24 статьи были отобраны для уместного и полнотекстового чтения. Из этого в общей сложности девятнадцать исследований были исключены из дальнейшей оценки. Семнадцать исследований были исключены, поскольку они сравнивали 1 л нового препарата для кишечника на основе полиэтиленгликоля (NER1006) с 2 л ПЭГ-А, а еще 2 исследования, которые сравнивали без аскорбиновой кислоты, также были исключены.Наконец, в настоящий метаанализ были включены 5 подходящих исследований (рис. 1).
Из этого в общей сложности девятнадцать исследований были исключены из дальнейшей оценки. Семнадцать исследований были исключены, поскольку они сравнивали 1 л нового препарата для кишечника на основе полиэтиленгликоля (NER1006) с 2 л ПЭГ-А, а еще 2 исследования, которые сравнивали без аскорбиновой кислоты, также были исключены.Наконец, в настоящий метаанализ были включены 5 подходящих исследований (рис. 1).
3.2. Характеристики и качество исследований
Все 5 испытаний (обобщенные характеристики в таблице 1) были проведены в Корее. В экспериментальной группе в четырех исследованиях проводилась подготовка кишечника с использованием 1 л ПЭГ-АК плюс бисакодил, а в остальных использовалось дополнительное лекарственное средство с прукалопридом. В контрольной группе все пациенты получали 2 л препарата для кишечника с раздельными дозами ПЭГ-А. Из 5 исследований 4 были одноцентровыми исследованиями.Путем поиска оригинальных протоколов исследования, доступных в Информационной службе клинических исследований (CRIS) и Clinical Trials. gov, и тщательного изучения, исследователи использовали тот же раствор для подготовки кишечника (Coolprep®: хлорид натрия 2,691 г, хлорид калия 1,015 г, Безводный сульфат натрия 7,5 г, ПЭГ 3350 100 г, аскорбиновая кислота 4,7 г, аскорбат натрия 5,9 г). Было немного доказательств систематической ошибки публикации для первичного результата ( Egger ’ s test), и систематическая ошибка риска каждого исследования была представлена на рисунке 2.Качество доказательств первичного исхода было умеренным (Таблица S3).
gov, и тщательного изучения, исследователи использовали тот же раствор для подготовки кишечника (Coolprep®: хлорид натрия 2,691 г, хлорид калия 1,015 г, Безводный сульфат натрия 7,5 г, ПЭГ 3350 100 г, аскорбиновая кислота 4,7 г, аскорбат натрия 5,9 г). Было немного доказательств систематической ошибки публикации для первичного результата ( Egger ’ s test), и систематическая ошибка риска каждого исследования была представлена на рисунке 2.Качество доказательств первичного исхода было умеренным (Таблица S3).
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
ABPS: Шкала подготовки кишечника Арончика; BBPS: Бостонская шкала подготовки кишечника; Бис: бисакодил; FD: первая доза; LD: последняя доза; PEG-Asc: полиэтиленгликоль плюс аскорбиновая кислота; Пру: прукалоприд; РКИ: рандомизированное контролируемое исследование; 1 л: 1 л полиэтиленгликоля плюс аскорбиновая кислота с адъювантом; 2 л: 2 л полиэтиленгликоля плюс аскорбиновая кислота. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
3.3. Характеристики участников
Всего было проанализировано 10 групп подготовки кишечника у 1013 пациентов (503 в группе 1L PEG-AA и 510 в группе 2L PEG-A).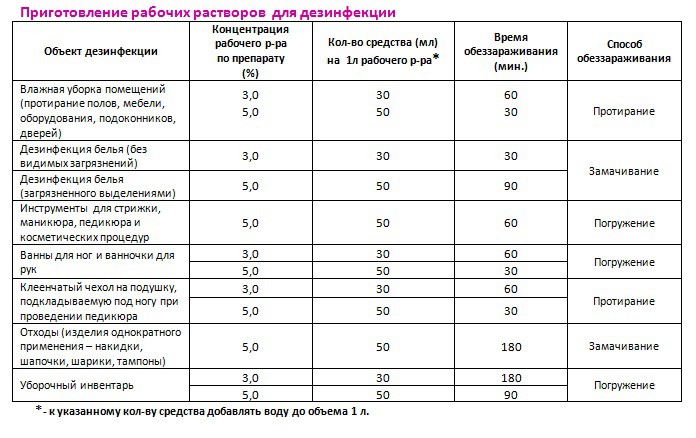 Доля пациентов мужского пола, индекс массы тела (ИМТ), частота предыдущих колоноскопий в анамнезе, источник пациентов, показания к колоноскопии, время процедуры и ограничения диеты были одинаковыми между двумя группами в индивидуальных испытаниях. CIR и ADR были удовлетворительными в обеих группах подходящих данных (таблица 1, таблица S4).
Доля пациентов мужского пола, индекс массы тела (ИМТ), частота предыдущих колоноскопий в анамнезе, источник пациентов, показания к колоноскопии, время процедуры и ограничения диеты были одинаковыми между двумя группами в индивидуальных испытаниях. CIR и ADR были удовлетворительными в обеих группах подходящих данных (таблица 1, таблица S4).
3.4. Первичный результат: эффективность (общая и сегментная толстая кишка)
Качество чистоты кишечника сообщалось в 5 испытаниях и оценивалось с помощью BBPS. В исследованиях, в которых представлены данные об адекватной скорости подготовки кишечника, режимы 1L PEG-AA продемонстрировали эквивалентную эффективность подготовки кишечника по сравнению с группой 2L PEG-A (89,3% против 89,4%; ОР 1,00; 95% ДИ 0,95–1,05. 😉 (Рисунок 3, Таблица 2).
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
указывает на неоднородность.ADR: частота выявления аденомы; BBPS: Бостонская шкала подготовки кишечника; CI: доверительный интервал; MD: средняя разница; для каждого анализа 95% Cl по MD / RR; RR: относительный риск. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
На основании данных об общем и сегменте ободочной кишки (правая, поперечная и левая ободочная кишка) не было очевидной разницы в эффективности между двумя препаратами для очищения кишечника (рис. S1-4, таблица 2). Однако значительная неоднородность (;) была обнаружена в левой ободочной кишке, и был проведен анализ подгрупп.Эффективность была несколько ниже в схемах 1 л ПЭГ-АК (MD -0,11; 95% ДИ -0,19-0,03; для гетерогенности 0,88) в подгруппе, потреблявшей только дополнительно 0,5 л воды.
3.5. Вторичные результаты
Другие показатели (общее время обследования и ADR), относящиеся к эффективности чистоты кишечника, были доступны. Никакой значительной тенденции к увеличению количества аденом (43,7% против 43,2%; ОР 1,01; 95% ДИ 0,86-1,18;) не было обнаружено в 2L PEG-A, чем 1L PEG-AA, при этом не было большой разницы в общем времени исследования (SMD — 0.86; 95% ДИ -1,88-0,15; ) (Таблица 2).
Данные о количестве пациентов с предпочтением были доступны в 3 из 5 групп лечения. В целом, 234/275 (85,1%) пациентов в группе 1L PEG-AA по сравнению с 190/280 (67,9%) в группе 2L PEG-A проявили готовность повторить те же схемы с объединенным RR 1,25 (95% ДИ). 1.14-1.38;) (Рисунок 4, Таблица 3). В двух исследованиях сообщается о сходных показателях завершения. Объединенный RR составил 1,03 (95% ДИ 0,95–1,07;) и не показал статистически значимых различий с низкой гетерогенностью.
В целом, 234/275 (85,1%) пациентов в группе 1L PEG-AA по сравнению с 190/280 (67,9%) в группе 2L PEG-A проявили готовность повторить те же схемы с объединенным RR 1,25 (95% ДИ). 1.14-1.38;) (Рисунок 4, Таблица 3). В двух исследованиях сообщается о сходных показателях завершения. Объединенный RR составил 1,03 (95% ДИ 0,95–1,07;) и не показал статистически значимых различий с низкой гетерогенностью.
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| указывает на неоднородность.CI: доверительный интервал; для каждого анализа 95% Cl по MD / RR; RR: относительный риск. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Во всех исследованиях сообщалось о нескольких аналогичных осложнениях (таких как тошнота, вздутие живота, рвота и боль в животе), которые были извлечены и проанализированы. Однако последнее исследование сочетало тошноту и рвоту, поэтому отдельные данные извлечь не удалось. Тошнота с 14,5% (118/815) и вздутие живота с 14,8% (150/1013) были более частыми осложнениями, чем другие, в то время как частота не показала статистической значимости в двух группах (соответственно ОР для тошноты 1.22 (95% ДИ 0,89–1,65),; ОР вздутия живота 0,96 (95% ДИ 0,73–1,28)). В контрольной группе о рвоте сообщалось реже и статистической значимости не наблюдалось (1,2% против 1,8%; ОР 0,69; 95% ДИ 0,32–1,50;). Никаких различий в отношении боли в животе в двух группах не наблюдалось (2,7% против 2,7%; ОР 1,01; 95% ДИ 0,61–1,69;) (Рис. S5-8, Таблица 3).
4. Обсуждение
Насколько нам известно, это первое метааналитическое исследование, в котором объединены подходящие индивидуальные данные из РКИ, сравнивающих 1 л PEG-AA с 2L PEG-Asc, а также определено качество подготовки кишечника с помощью оценки BBPS. как результат.Согласно нашему исследованию, основной результат показал, что эффективность и безопасность 1 л PEG-AA не уступала 2L PEG-A, но наблюдалась большая готовность пациентов повторять 1 л PEG-AA. Повышение готовности пациентов к подготовке кишечника важно для повышения частоты проведения колоноскопии и, таким образом, способствует предотвращению колоректального рака.
При описании качества подготовки BBPS считается наиболее тщательно проверенной шкалой [14] и предполагается, что она будет использоваться в клинических условиях для всех опубликованных шкал, показывающих ограничения [15].Кроме того, если в рейтинге для каждой колоноскопии участвует более одного оценщика, может быть рекомендована дихотомическая конечная точка [16]. Поэтому в качестве основного результата мы использовали адекватную скорость подготовки кишечника. Все эндоскописты в текущем исследовании были хорошо обучены устранению предвзятости и использовали BBPS для оценки на основе своего собственного опыта. Более того, всестороннее рассмотрение общих и сегментарных показателей толстой кишки также оставалось хорошим способом подтверждения результатов сравнения различий в подготовке кишечника.
В включенных исследованиях индивидуально оценивалась эффективность адъювантных препаратов в снижении количества растворов препаратов для кишечника: одно — с прукалопридом [17], а остальные четыре — с бисакодилом [18–21]. В нашем обзоре подчеркнута возможность использования комбинации для подготовки кишечника после обобщения результатов (первичных или вторичных) у 1013 пациентов. Результаты не показали значительных недостатков в группе с меньшим объемом. В то время как для чистоты левой кишки Kang et al.[19] и Kim et al. [21] обнаружили, что прямая и сигмовидная кишка была более статистически эффективной в группе 1L PEG-AA (2,57 против 2,26). Помимо расхождений в статистических выводах, были изучены источники неоднородности в рамках исследования и было замечено, что это могло быть связано с добавлением разных количеств воды и дополнительным 1 л воды, введенным в качестве последней дозы по сравнению с 0,5 л. в других исследованиях (таблица 1). Было бы очень интересно оценить, может ли дополнительная вода без приема слабительного повлиять на чистоту кишечника.Другим объяснением может быть разница в дозировке и типе использования адъюванта.
Кроме того, на подготовку кишечника влияют многие факторы, связанные с пациентом, что неизбежно приводит к неоднородности. Как показали несколько предыдущих исследований, такие предикторы, как возраст, пол, ИМТ, предыдущая история колоноскопии, диетические ограничения, различие в марке лекарств, показания к проведению колоноскопии и интервал времени до процедуры, показали связь с очищением толстой кишки [22, 23 ]. Почти все исследования, включенные в этот метаанализ, были внутренне согласованными в этих отношениях, чтобы исключить влияние этих смешивающих факторов на результаты.Тем не менее, в исследовании Кима наблюдалась статистически значимая разница в среднем возрасте пациентов [20]. Результаты нашего исследования показали, что пациенты в группе 2L (48,14 против 52,88) были моложе, что не соответствовало общепринятому пороговому значению, и результаты в конечном итоге не показали значительной разницы между двумя группами [22].
Тем не менее, согласно стандарту подготовки кишечника, мы считаем, что балл BBPS ≥2 для всех сегментов и / или в целом является достаточным [24]. Хотя в руководстве указано, что минимальный стандарт ≥90% для адекватной подготовки кишечника, оцененный с использованием проверенных шкал, может достичь только меньшинство центров, а в литературе указано, что уровень неадекватной подготовки кишечника в настоящее время составляет от 5% до 30%. [2, 25].Уровень АД в этом исследовании с объединенным показателем 89% колебался от 83% до 96%, все из которых находились на среднем и верхнем уровне в клинической практике. Более того, показатели ADR и CIR были выше минимального стандарта (,) для колоноскопии в каждом исследовании в соответствии с текущими рекомендациями (Таблица S4) [2]. Возможно, пока слабительное принимается в определенной дозе, другие аспекты, вызывающие беспокойство, а не доза, могут играть более важную роль в подготовке кишечника.
Еще одним заметным преимуществом этого протокола является готовность пациентов к повторению, набор достаточного количества пациентов и явно продемонстрированное предпочтение схемам с более низкими дозами [26].Режим с более низкими дозами, при котором большое количество раствора заменяется адъювантом за день до колоноскопии, особенно использование дополнительных суппозиториев в день колоноскопии, может уменьшить нарушение сна [20]. Во-вторых, он снижает потребление этих невкусных жидкостей, что может снизить психологическую нагрузку на пациентов. Желание пациентов должно быть высоко оценено, несмотря на одинаковые показатели завершения у пациентов, и не следует поощрять подход с высокой степенью подготовки для всех [27–29].
Осложнения пациентов в основном были связаны с наиболее частыми побочными эффектами, включая тошноту, рвоту, боль в животе и диарею [30]. Результаты этого исследования не показали статистических различий, в то время как можно сделать только консервативную оценку из-за ограниченного размера выборки в этой части. Основываясь на имеющейся в настоящее время литературе, наши результаты подтверждают использование дополнительных адъювантов только с раствором PEG-Asc [17–21]. Согласно гипотезе, катартическое действие бисакодила и прукалоприда может быть связано с его катарсическим или прокинетическим механизмом, который, в свою очередь, изменяет двигательные паттерны в толстой кишке и способствует движению кишечника [31, 32].
В настоящее время скорость адекватной подготовки кишечника значительно улучшилась клинически [29], но опыт приема слишком большого количества слабительных средств по-прежнему остается серьезной проблемой. Роль адъювантов в низком объеме PEG-Asc неясна, и в текущих рекомендациях говорится, что использование прокинетических агентов обычно не рекомендуется [5]. Таким образом, они не нашли широкого применения в повседневной клинической практике. Несмотря на ограниченное количество опубликованных данных в некоторых исследованиях, этот обзор свидетельствует об отсутствии очевидных недостатков в отношении эффективности и безопасности схем лечения 1 л ПЭГ-АА у амбулаторных пациентов.
Наш анализ включал нескольких пациентов, а также обнаружил приемлемую гетерогенность в большинстве сравнений по основным исходам. Следует отметить некоторые ограничения в этом исследовании. Во-первых, было включено меньшее количество исследований, и все исследования были взяты из одной страны; поэтому обобщаемость результатов сомнительна и требует дополнительных исследований для проверки результатов. Во-вторых, не все детали, представленные в этом исследовании, были проанализированы из-за ограниченной информации о вкусовых качествах и общем дискомфорте, которые могли иметь значение, но не иметь клинического значения.В-третьих, почти все включенные популяции были амбулаторными, и, учитывая эти ограничения, результаты нашего исследования следует применять с осторожностью. Согласно предыдущему исследованию, услуги амбулаторной помощи оставались фактором низкого риска, что указывает на то, что 1 л PEG-AA может быть более подходящим для населения с низким риском [33]. Наконец, в качестве вспомогательных препаратов использовались только бисакодил и прукалоприд, и необходимы дальнейшие исследования для изучения эффективности сочетания других препаратов, таких как пробиотики, мозаприд, цитрат магния и касторовое масло, с 1 л PEG-Asc.
5. Заключение
В заключение, ПЭГ в небольшом объеме с адъювантами можно рассматривать как альтернативу традиционному ПЭГ в низких дозах (2 л) для подготовки кишечника перед колоноскопией. Дальнейшие усилия должны быть сосредоточены на большем количестве подходов к снижению потребления слабительных. В это исследование предпочтительно включить около 1863 пациентов (со снижением риска на 10%).
Раскрытие информации
Предварительный отчет был представлен в виде плаката на Международном форуме по болезням пищеварения 2020 г. (IDDF).
Конфликт интересов
Авторы заявляют об отсутствии конкурирующих интересов.
Вклад авторов
Синь Юань и Чжисинь Чжан — равные участники.
Благодарности
Авторы благодарят Medjaden Bioscience Limited за редакционные советы. Это исследование было поддержано Проектом медицинских наук и технологий в области здравоохранения Комиссии здравоохранения провинции Чжэцзян (№ 2016KYB257 и 2017KY581).
Дополнительные материалы
Таблица S1: Стратегия поиска EMBASE.Таблица S2: исходные наборы данных. Таблица S3: Сводка результатов GRADE. Таблица S4: исходные характеристики пациентов. Рисунок S1-S4: сравнение лесных участков по общему количеству BBPS и сегментному баллу между 1L PEG-AA и 2L PEG-A. Фигура S5-S8: сравнение лесного графика частоты нежелательных явлений между 1 л PEG-AA и 2L PEG-A. Средневзвешенная разница (WMD) и 95% доверительный интервал (CI) эффективности толстой кишки согласно шкале BBPS. Относительный риск (ОР) и 95% ДИ нежелательных явлений. 1 л ПЭГ-АК относится к 1 л полиэтиленгликоля плюс аскорбиновая кислота с адъювантным лекарственным средством; 2 л ПЭГ-А означает 2 л полиэтиленгликоля плюс аскорбиновая кислота. (Дополнительные материалы)
Как косметолог может продезинфицировать стерилизатор?
Коробка для УФ-стерилизатора DIY : Как косметолог может дезинфицировать инструменты с помощью коробки для стерилизатора?В этой статье будет обсуждаться одна из очень важных тем — как выбрать самодельный УФ-стерилизатор бокс ?
Мастера обычно проводят следующие работы по чистке и дезинфекции маникюрных наборов:
- Дезинфекция — это уничтожение возбудителей инфекционных заболеваний и уничтожение токсинов в окружающей среде.Дезинфекция снижает количество микроорганизмов до приемлемого уровня, но не может полностью уничтожить их
- предстерилизационная очистка — процесс удаления механических, жировых и белковых отложений и остатков лекарств.
- Стерилизация — это освобождение объекта или материала от ВСЕХ типов микроорганизмов. Он включает бактерии и их споры, грибы и вирусы. Вы можете найти их в основном на поверхности и внутри продуктов . Бокс уф-стерилизатора своими руками — это полное избавление от живых микроорганизмов.
- Дополнительная обработка, включающая дезинфекцию рук мастера, клиента, а также рабочих поверхностей и помещений.
Обычно в профессиональных салонах красоты предстерилизационную очистку проводят с помощью diy УФ-стерилизатор . В основном это современные дезинфицирующие средства, например, Аламинол . Для этого инструменты погружаются в раствор на время, указанное в инструкции.Существуют различные простые методы дезинфекции устройств. Орех теперь, у нас есть новейшие технологии. Это предотвращает попадание микробов на поверхность устройства.
Сегодня специалисты ногтевого сервиса используют различные типы diy УФ-стерилизатор . Потому что эти устройства обеспечивают отличную производительность.
По своей сути стерилизатор — это устройство, которое воздействует на маникюрные инструменты с различным излучением или иным образом. Таким образом, легко убить бактерии и микробы, присутствующие на них.
Рассмотрим основные виды бокс-стерилизатора своими руками уфСтерилизатор Glasperlen (шариковый, кварцевый)
В целом, он идеален для использования в маникюрных и косметических салонах, а также для мастеров в домашних условиях. Шариковый стерилизатор дезинфицирует инструменты, подвергая их воздействию высоких температур — 250 градусов Цельсия. В кварцевом стерилизаторе работают разные инструменты. Кроме того, это устройство полностью уничтожает микробы.
Устройствам очень трудно переносить бактерии после diy УФ-стерилизатор . В таком устройстве, благодаря воздушному способу нагрева кварцевых шариков, происходит глубокая стерилизация.
Преимущества кварцевого стерилизатора:
- Компактный, устойчивый.
- Быстро нагревается до температуры стерилизации.
- Имеет самое короткое время стерилизации, всего 15-20 секунд. При высокотемпературной обработке (до 250 ° С) инструментов время обработки составляет до 180 секунд.
- Длительный срок службы.
- Не дорого.
- Не потребляет много энергии.
Стерилизации подлежит только рабочая поверхность инструмента. Точно так же нарушается кожа (т.е. ручки остаются не стерилизованными, так как кварц может их повредить).
Рабочую поверхность окунуть в кварц, т.е. песок. Точно так же он действует как абразив и не затачивает инструмент, а затупляет его.
- Подходит только для инструментов из жаропрочного металлического сплава.
- Деталь, требующая ежегодной замены — кварцевые шары.
Подходит для цельнометаллических инструментов:
Один из самых распространенных и эффективных методов дезинфекции, основное действие которого — термическая обработка. Этот стерилизатор для уф-стерилизатора diy достигает около 200-260 градусов Цельсия. Эффективность стерилизации напрямую зависит от свободного доступа воздуха к обрабатываемым объектам.Поэтому необходимо соблюдать правильную загрузку камеры.
Преимущества сухой печи:
- Вся поверхность инструмента стерилизована.
- Сушильный шкаф может работать в нескольких температурных режимах — в разных моделях максимальная температура достигает 160-260 ° С.
- Горячий сухой воздух в сухом тепле исключает коррозию металлических инструментов и эрозию стеклянных поверхностей. Следовательно, это позволяет им сохранять свою целостность и физические свойства.
- Стерилизующим агентом в данном случае является сухое тепло. Кроме того, он обладает отличными проникающими свойствами практически для любого материала.
- Высокая цена.
- Длительное время стерилизации. Время обработки зависит от модели устройства, выбранной температуры. Кроме того, он может варьироваться от 30 до 120 минут.
- Необходимость использования негорючих упаковочных материалов для стерилизуемого инструмента.Исключая бумагу, пергамент, необработанную бязь и некоторые другие. Также исключены резина, текстиль, полимеры и другие аксессуары, не выдерживающие высоких температур.
- Перед стерилизацией убедитесь, что предметы термостойкие.
Обычно специальные крафт-пакеты являются общими для diy УФ-стерилизатора . Он надолго сохраняет асептическое состояние инструмента или материала. 21-60 дней (в зависимости от марки производителя) при застегивании с клапаном.
Коробка для ультрафиолетового стерилизатораЭто важная и незаменимая вещь. Обычно для дезинфекции и хранения уже стерилизованных инструментов используется:
- Маникюр
- салона красоты и салона
- парикмахерские
Идеально подходит для инструментов, которые не переносят высокие температуры (гребни, напильники, бафы, губки). Под воздействием ультрафиолета гибнет грибковая и бактериальная флора.
УФ-стерилизаторыбывают одно- или двухкамерные. Впоследствии ассортимент можно найти здесь .
Преимущества УФ-стерилизатора:- Стоимость данного аппарата ниже, чем у термообработанного аппарата.
- УФ-лампы можно легко заменить.
- Отлично подходит для дополнительной оснастки.
- Бокс для УФ-стерилизатора своими руками дезинфицирует материалы, которые нельзя стерилизовать другими методами.Точно так же УФ не влияет на их качество.
Недостатки УФ-стерилизатора:
- Длительное время обработки, всего 40 минут на партию. Облучение одной стороны инструмента занимает 15-20 минут. Это время может незначительно отличаться в зависимости от модели машины.
- Не стерилизует (только дезинфекция инструмента!)
- Он больше подходит для хранения инструмента после стерилизации.
Используется для чистки мелких предметов — боров, фрез и других инструментов для обработки ногтей. Ультразвуковые волны заставляют жидкость в контейнере вибрировать. Такой метод позволяет очистить поверхность от грязи и ржавчины даже в труднодоступных местах.
Обработки в таком устройстве недостаточно для полного уничтожения всех бактерий. Поэтому ультразвук используется как подготовка к термообработке.Затем для основной дезинфекции используются кварцевые стерилизаторы или сушильные шкафы. Но в уборке загрязненных труднодоступных мест ему действительно нет равных.
Преимущества ультразвуковых стерилизаторов:
- Ультразвуковая мойка в восемь раз эффективнее горячей дезинфекции в растворах — она удаляет с инструментов бактерии, патогенные микроорганизмы, грязь и ржавчину.
- Идеально подходит для маникюрных инструментов из разных материалов — всех видов металла, пластика, стекла, керамики.
- Инструменты при обработке в стерилизаторах не деформируются, не корродируют и не тупятся.
- Скорость стерилизации. Даже самый загрязненный инструмент стерилизуется не более чем за 10 минут.
- Полностью безопасен для работы. В отличие от термообработки здесь нет риска ошпаривания.
- В нем можно не только стерилизовать, но и хранить инструменты до следующего использования.
- Кроме того, он предлагает доступную цену.
При активной работе через руки мастеров педикюра и маникюра проходит огромное количество людей.Хранение лучшего diy УФ-стерилизатор может спасти людей от множества микробов. Особенно в covid 19 вам нужно обезопасить свое окружение. Более того, вы можете сделать это, просто купив новый контейнер для УФ-стерилизатора diy. Так что каждый уважающий себя специалист должен выполнять свою деятельность не только качественно, но и максимально безопасно.
Мета-анализ рандомизированных контролируемых исследований
Abstract
Эффективность дополнительного использования адъювантов для подготовки кишечника все еще неясна.В этом исследовании сравнивали 1 л полиэтиленгликоля плюс аскорбиновая кислота с режимами адъювантных препаратов (1 л ПЭГ-АА, меньший объем) с 2 л полиэтиленгликоля плюс аскорбиновая кислота (2 л ПЭГ-А, низкий объем), чтобы оценить, можно ли использовать адъюванты для снижения стандарта. дозировка слабительного дальше. В базе данных PubMed / MEDLINE, EMBASE, Cochrane Library и Web of Science был проведен поиск рандомизированных контролируемых испытаний (РКИ). Первичным результатом была эффективность подготовки кишечника, а вторичными результатами — переносимость пациентами и частота осложнений.Общее качество доказательств оценивалось с помощью инструмента разработки рекомендаций GRADEpro. Были включены пять РКИ с участием 1013 пациентов из Кореи. Большинство пациентов были амбулаторно из разных больниц. Объединенные данные не показали существенной разницы в частоте адекватной подготовки кишечника (89,3% против 89,4%, ОР 1, 95% ДИ 0,95–1,05, I 2 = 47%), а также в частоте осложнений (ОР для тошнота 1,22, 95% ДИ 0,89-1,65, I 2 = 49%; ОР для вздутия живота 0.96, 95% ДИ 0,73–1,28, I 2 = 0%; ОР при рвоте 0,69, 95% ДИ 0,32–1,50, I 2 = 33%; ОР боли в животе 1,01, 95% ДИ 0,61–1,69, I 2 = 0%). Но значительно более высокая степень готовности наблюдалась в меньшем объеме (85,1% против 67,9%, ОР 1,25, 95% ДИ 1,14–1,38, I 2 = 46%). Качество доказательств первичного исхода было умеренным. Результаты этого метаанализа показали, что 1 л PEG-AA может быть жизнеспособной альтернативой 2L PEG-A со сравнимой эффективностью, лучшими предпочтениями пациентов и отсутствием статистически значимых нежелательных явлений.
1. Введение
Колоноскопия имеет важное клиническое значение в профилактике колоректального рака [1]. Подчеркивается важность качества подготовки кишечника, поскольку это один из семи ключевых показателей эффективности, рекомендованных для колоноскопии Комитетом по качеству Европейского общества эндоскопии желудочно-кишечного тракта (ESGE) [2]. Однако до колоноскопии пациентов в основном беспокоила сама колоноскопия; страх перед колоноскопией сопровождался подготовкой кишечника [3, 4].
Существуют различные коммерчески доступные средства подготовки кишечника для его очищения. Кроме того, руководящие принципы рекомендуют препараты на основе полиэтиленгликоля (ПЭГ) в больших или малых объемах, а также препараты, не содержащие ПЭГ; они требуют клинической проверки для рутинной подготовки кишечника [5]. Принимая во внимание, что из-за более низкой стоимости схемы на основе 2-4 л ПЭГ являются предпочтительным методом и широко используются с момента появления раствора ПЭГ в 1980 году [6]. Объем раствора препарата считается основной проблемой переносимости и приемлемости пациентов, готовящихся к колоноскопии [7].
Вопросы плохой комплаентности и объема низкой переносимости слабительных средств при подготовке кишечника уже были рассмотрены. Уменьшение объема ПЭГ в методе 2 л ПЭГ плюс аскорбиновая кислота (ПЭГ-Asc) является безопасным и эффективным методом подготовки кишечника по сравнению с традиционным методом 4 л ПЭГ [8, 9]. В результате метод 2L PEG-Asc теперь рассматривается как действительная альтернатива стандартному PEG и одобрен Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США [10]. Однако дозировка этого режима все еще велика для приема внутрь.Кроме того, показано, что с предварительно упакованной диетой с низким содержанием остатков режим 1 л PEG-Asc не уступает раствору в небольшом объеме с точки зрения очищающей эффективности [11]. Для общей подготовки кишечника, хотя адъюванты, за исключением симетикона, не рекомендуются для рутинного использования [5, 12, 13], несколько недавних исследований в Корее показали, что дополнительное использование вспомогательного вещества вместе с традиционными средствами подготовки кишечника может уменьшить требуемый объем. .
В текущем обзоре сравнивается эффективность 1 л ПЭГ с аскорбиновой кислотой плюс дополнительные лекарственные препараты (1 л ПЭГ-АА, меньший объем) с 2 л ПЭГ с режимами аскорбиновой кислоты (2 л ПЭГ-А, низкий объем) с использованием метааналитических методов.Это исследование направлено на изучение возможности использования дополнительных препаратов для PEG-Asc для снижения дозировки слабительного у большего числа пациентов.
2. Методы
2.1. Источники данных и стратегия поиска
Систематический поиск был выполнен двумя независимыми рецензентами (Синь Юань и Чжисинь Чжан) через PubMed / MEDLINE, EMBASE, Кокрановскую библиотеку и Web of Science (до 10 марта 2020 г.) с предварительно определенными условиями поиска. Стратегия поиска (пример EMBASE в таблице S1) была сформулирована в соответствии с заголовком / входом медицинских предметов вместе с ключевыми словами, относящимися к «колоноскопия», «полиэтиленгликоль» и «1L.”Были включены только полные тексты, опубликованные на английском языке.
После удаления повторяющихся исследований с помощью встроенной функции в программе EndNote были проверены заголовки и аннотации, а затем полные тексты потенциально релевантных исследований были проверены на соответствие критериям. Чтобы избежать упущения в литературе, мы также просмотрели ссылки на каждую литературу.
2.2. Критерии приемлемости исследования
Исследования были признаны подходящими согласно критериям PICOS: (1) участники (P): все взрослые, которым была сделана колоноскопия; (2) вмешательства (I) и сравнения (C): сравнение 1 л PEG-AA с 2 л PEG-A перед колоноскопией; (3) результат (O): первичный результат включает эффективность подготовки кишечника, измеренную по Бостонской шкале подготовки кишечника (BBPS), а вторичные результаты включают переносимость и осложнения, связанные с режимом; и (4) исследование (S): рандомизированные контролируемые испытания (РКИ).
2.3. Синтез данных
Основные характеристики (такие как возраст, пол, сопутствующие заболевания, показания к колоноскопии и меры по подготовке кишечника), показатели качества (общее время обследования, частота выявления аденомы (ADR), количество опытных эндоскопистов, частота интубации слепой кишки ( CIR)), а исходы (такие как частота адекватной подготовки кишечника (АД), общий балл и баллы по сегментам BBPS, переносимость и осложнения) были извлечены из соответствующих статей двумя независимыми исследователями (Xin Yuan и Lu Xu).Исходные наборы данных представлены в таблице S2. Любые разногласия между следователями разрешались арбитражем и разрешались путем взаимного обсуждения, и достигалось соглашение с помощью старшего следователя (Лэй Сюй).
2.4. Риск систематической ошибки и оценка достоверности
Качество исследования оценивалось с использованием инструмента Cochrane Collaboration для оценки риска систематической ошибки для РКИ. Инструмент включал семь областей оценки (таких как генерация случайной последовательности, сокрытие распределения, слепота участников и персонала, слепая оценка результатов, неполные данные, выборочная отчетность и другие систематические ошибки) и классифицируются как низкий, неясный или высокий риск.Из-за включения ограниченных исследований систематическая ошибка публикации оценивалась не с помощью воронкообразной диаграммы, а с помощью теста Эггера. Достоверность исследования оценивалась одним из авторов (Вейхонг Ван) с использованием подхода GRADEpro GDT (https: // gdt. Http://gradepro.org/app) для обобщения качества доказательств.
2,5. Статистический анализ
Извлеченные данные были последовательно собраны во всех подходящих исследованиях, объединены и сведены в таблицу в едином формате в Microsoft Excel.Статистический анализ проводился с использованием программного обеспечения RevMan (Review Manager, версия 5.3) и программного обеспечения STATA (StataMP, версия 14). Поскольку наш метаанализ включал переменные непрерывности, то есть оценку BBPS и дихотомические переменные, то есть готовность к повторению, они были отдельно рассчитаны и отображены с использованием лесных участков с фиксированной или случайной моделью эффектов. Для дихотомических событий был рассчитан относительный риск (ОР) вместе с 95% доверительным интервалом (ДИ). Поскольку включенные исходы были непрерывными переменными, объединенные оценки были рассчитаны как средние различия (MD), а также 95% доверительный интервал.Статистическая неоднородность испытаний оценивалась с помощью показателя несогласованности I 2 и значения P , которое было значимым, если I 2 составляло> 50% или P <0,10. Если статистически значимо, то анализ исключения исследования проводился, когда наблюдались возможные источники клинической гетерогенности определенного исследования, и применялась модель случайных эффектов. Кроме того, при необходимости проводился анализ подгрупп.
3. Результаты
3.1. Результаты поиска
Первоначальное исследование литературы дало 306 статей, 147 из которых были немедленно исключены из-за дублирования. Затем, после обзора названий и аннотаций, в общей сложности 135 исследований были отклонены, потому что они были либо неколоноскопическими исследованиями, либо отсутствием полных текстов, либо не сравнивали рассматриваемые препараты кишечника. После этого 24 статьи были отобраны для уместного и полнотекстового чтения. Из этого в общей сложности девятнадцать исследований были исключены из дальнейшей оценки.Семнадцать исследований были исключены, поскольку они сравнивали 1 л нового препарата для кишечника на основе полиэтиленгликоля (NER1006) с 2 л ПЭГ-А, а еще 2 исследования, которые сравнивали без аскорбиновой кислоты, также были исключены. Наконец, в настоящий метаанализ были включены 5 подходящих исследований ().
Блок-схема поиска литературы (PEG-Asc: полиэтиленгликоль с аскорбиновой кислотой; PEG-ELS: полиэтиленгликоль).
3.2. Характеристики и качество исследований
Все 5 испытаний (обобщенные характеристики приведены в) были проведены в Корее.В экспериментальной группе в четырех исследованиях проводилась подготовка кишечника с использованием 1 л ПЭГ-АК плюс бисакодил, а в остальных использовалось дополнительное лекарственное средство с прукалопридом. В контрольной группе все пациенты получали 2 л препарата для кишечника с раздельными дозами ПЭГ-А. Из 5 исследований 4 были одноцентровыми исследованиями. Путем поиска оригинальных протоколов исследования, доступных в Информационной службе клинических исследований (CRIS) и Clinical Trials.gov, и тщательного изучения, исследователи использовали тот же раствор для подготовки кишечника (Coolprep®: Sodium Chloride 2.691 г, хлорид калия 1,015 г, безводный сульфат натрия 7,5 г, ПЭГ 3350 100 г, аскорбиновая кислота 4,7 г, аскорбат натрия 5,9 г). Было немного доказательств систематической ошибки публикации для первичного результата ( Egger ‘ s test P = 0,441), и систематическая ошибка риска каждого исследования была представлена в. Качество доказательств первичного исхода было умеренным (Таблица S3).
Таблица 1
Исходные характеристики включенных рандомизированных контролируемых исследований.
| Исследование, год (страна) | Источник пациентов | Экспериментальные группы | 1L, n | 2L, n | Использование адъюванта | Время первой и последней дозы | время | Диета | Результаты | Тип исследования | |
|---|---|---|---|---|---|---|---|---|---|---|---|
| Kwon et al.[18], 2016 (Корея) | Амбулаторно | FD: Bis + 0,5 л воды LD: 1 л PEG — Asc + 0,5 л воды | 91 | 96 | 20 мг бисакодила | FD: 20 часов в день — до ЛД: 6 часов утра — из | ≥3 ч интервал до | 3-дневный низкий остаток | BBPS | Многоцентровое, простое слепое, РКИ | |
| Kang et al. [19], 2017 (Корея) | Амбулаторное лечение | FD: Bis LD: 1 л PEG — Asc + 1 л воды | 100 | 100 | 10 мг бисакодила | FD: 9 вечера накануне LD : ≥4 ч до | 9: 00-13: 00 | 3-дневный низкий остаток | BBPS, ABPS | Одноцентровое, простое слепое, РКИ | |
| Choi et al.[17], 2019 (Корея) | Амбулаторно | FD: Pru + 0,5 л воды LD: 1 л PEG — Asc + 0,5 л воды | 130 | 130 | 2 мг прукалоприда | FD: 19:00 в день -prior LD: ≥5 ч до | 9: 00-13: 00 | 3-дневный низкий остаток | BBPS, ABPS | Одноцентровое, простое слепое, РКИ | |
| Kim et al. [20], 2019 (Корея) | Амбулаторно | FD: — LD: Bis + 1 л PEG — Asc + 0,5 л воды | 83 | 85 | 20 мг бисакодила (суппозиторий) | FD: — LD: 5:00 в день | 8:30 до 12:00 | Прозрачная жидкость на 1 день | BBPS | Одноцентровое, одинарное слепое исследование, RCT | |
| Kim et al.[21], 2020 (Корея) | NA | FD: Bis LD: 1 л PEG — Asc + 1 л воды | 99 | 99 | 10 мг бисакодила | FD: в 21:00 предыдущего дня LD : ≥5 ч до | 9: 00-17: 00 | 3-дневный низкий остаток | BBPS | Одноцентровое, простое слепое исследование, RCT |
3.3. Характеристики участников
Всего было проанализировано 10 групп подготовки кишечника у 1013 пациентов (503 в 1 л PEG-AA и 510 в 2 л PEG-A).Доля пациентов мужского пола, индекс массы тела (ИМТ), частота предыдущих колоноскопий в анамнезе, источник пациентов, показания к колоноскопии, время процедуры и ограничения диеты были одинаковыми между двумя группами в индивидуальных испытаниях. CIR и ADR были удовлетворительными в обеих группах подходящих данных (Таблица S4).
3.4. Первичный результат: эффективность (общая и сегментная толстая кишка)
Качество чистоты кишечника сообщалось в 5 испытаниях и оценивалось с помощью BBPS. В исследованиях, в которых представлены данные об адекватной скорости подготовки кишечника, режимы 1L PEG-AA продемонстрировали эквивалентную эффективность подготовки кишечника по сравнению с группой 2L PEG-A (89.3% против 89,4%; 1,00 руб .; 95% ДИ 0,95–1,05; I 2 = 47%) (,).
Сравнение лесного графика адекватной скорости подготовки кишечника между 1 л ПЭГ-АК и 2 л ПЭГ-А (ОР: относительный риск; ДИ: доверительный интервал; 1 л ПЭГ-АК относится к 1 л полиэтиленгликоля плюс аскорбиновая кислота с адъювантным препаратом; 2 л ПЭГ-А относится к 2 л полиэтиленгликоля плюс аскорбиновая кислота).
Таблица 2
Анализ результатов первичного исхода и влияния на процедуру с точки зрения эффективности очищения.
| Эффективность | Количество исследований | n | MD / RR | 95% ДИ | P | I 2 | P значение неоднородности | ||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Адекватная скорость подготовки кишечника | 4 | 845 | 1,00 | 0,95 ~ 1,05 | 0,87 | 47% | 0,13 | PS | |||||
| Правая кишка | 5 | 1013 | -0.07 | -0,15 ~ 0,01 | 0,13 | 16% | 0,31 | ||||||
| Поперечная кишка | 5 | 1013 | 0,03 | -0,04 ~ 0,10 | 0,39 | 0% | 0,5 | ||||||
| Левая кишка | 5 | 1013 | 0,05 | -0,14 ~ 0,24 | 0,62 | 86% | <0,001 | ||||||
| Всего | 5 | 1013 | 0.01 | -0,17 ~ 0,18 | 0,83 | 36% | 0,18 | ||||||
| Общее время обследования | 4 | 826 | -0,86 | -1,88 ~ 0,15 | 0,14 | 0,2 | |||||||
| ADR | 4 | 826 | 1,01 | 0,86 ~ 1,18 | 0,91 | 0% | 0,60 |
На основе данных общего и сегментного ободочной кишки (правого, поперечного и левого) толстой кишки), не было очевидной разницы в эффективности между двумя препаратами для очищения кишечника (рис. S1-4,).Однако значительная неоднородность ( I 2 = 86%; P <0,0001) была обнаружена в левой ободочной кишке, и был проведен анализ подгрупп. Эффективность была несколько ниже в схемах 1 л ПЭГ-АК (MD -0,11; 95% ДИ -0,19-0,03; I 2 = 0%; P для гетерогенности 0,88) в подгруппе только дополнительных 0,5 л воды. потребление.
3.5. Вторичные результаты
Другие показатели (общее время обследования и ADR), относящиеся к эффективности чистоты кишечника, были доступны.Никакой существенной тенденции к увеличению количества аденом (43,7% против 43,2%; ОР 1,01; 95% ДИ 0,86-1,18; I 2 = 0%) не было обнаружено в 2L PEG-A, чем 1L PEG-AA, не проявляя особого влияния. разница в общем времени обследования (SMD -0,86; 95% ДИ -1,88-0,15; I 2 = 27%) ().
Данные о количестве пациентов с предпочтением были доступны в 3 из 5 групп лечения. В целом, 234/275 (85,1%) пациентов в группе 1L PEG-AA по сравнению с 190/280 (67,9%) в группе 2L PEG-A проявили готовность повторить те же схемы с объединенным RR, равным 1.25 (95% ДИ 1,14–1,38; I 2 = 46%) (,). В двух исследованиях сообщается о сходных показателях завершения. Объединенный RR составил 1,03 (95% ДИ 0,95–1,07; I 2 = 8%) и не показал статистически значимых различий с низкой гетерогенностью.
Сравнение лесного графика готовности 1 л ПЭГ-АА по сравнению с 2 л ПЭГ-А (ОР: относительный риск; ДИ: доверительный интервал; 1 л ПЭГ-АК относится к 1 л полиэтиленгликоля плюс аскорбиновая кислота с адъювантным препаратом; 2 л ПЭГ-А относится к 2 л полиэтиленгликоля плюс аскорбиновая кислота).
Таблица 3
Анализ результатов для вторичных исходов с точки зрения опыта пациентов.
| Переносимость и безопасность | Количество исследований | n | RR | 95% ДИ | P | I 2 | P значение неоднородности | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Переносимость | |||||||||||||||
| Готовность повторить | 3 | 1 555 | 9251,14 ~ 1,38 | <0,001 | 46% | 0,16 | |||||||||
| Степень выполнения | 2 | 447 | 1,03 | 0,98 ~ 1,07 | 0,21 | 8% | 0,3072 | Безопасность | |||||||
| Тошнота | 4 | 815 | 1,22 | 0,89 ~ 1,65 | 0.21 | 49% | 0,12 | ||||||||
| Рвота | 4 | 815 | 0,69 | 0,32 ~ 1,50 | 0,35 | 33% | 0,21 | ||||||||
| Боль в животе | 1,01 | 0,61 ~ 1,69 | 0,06 | 0% | 0,72 | ||||||||||
| Полнота / вздутие живота | 5 | 1013 | 0,96 | 0,73 ~ 1,28 | 0.80 | 0% | 0,63 |
Во всех исследованиях сообщалось о нескольких аналогичных осложнениях (таких как тошнота, вздутие живота, рвота и боль в животе), которые были извлечены и проанализированы. Однако последнее исследование сочетало тошноту и рвоту, поэтому отдельные данные извлечь не удалось. Тошнота с 14,5% (118/815) и вздутие живота с 14,8% (150/1013) были более частыми осложнениями, чем другие, в то время как частота не показала статистической значимости в двух группах (соответственно ОР для тошноты 1.22 (95% ДИ 0,89–1,65), I 2 = 49%; ОР для вздутия живота 0,96 (95% ДИ 0,73–1,28), I 2 = 0%). О рвоте меньше сообщалось, и статистической значимости не наблюдалось в контрольной группе (1,2% против 1,8%; ОР 0,69; 95% ДИ 0,32–1,50; I 2 = 33%). Никаких различий в отношении боли в животе в двух группах не наблюдалось (2,7% против 2,7%; ОР 1,01; 95% ДИ 0,61–1,69; I 2 = 0%) (Рис. S5-8,).
4.Обсуждение
Насколько нам известно, это первое метааналитическое исследование, в котором объединились подходящие индивидуальные данные из РКИ, сравнивающих 1 л PEG-AA с только 2 L PEG-Asc, а также определено качество подготовки кишечника с оценкой BBPS в качестве результата. Согласно нашему исследованию, основной результат показал, что эффективность и безопасность 1 л PEG-AA не уступала 2L PEG-A, но наблюдалась большая готовность пациентов повторять 1 л PEG-AA. Повышение готовности пациентов к подготовке кишечника важно для повышения частоты проведения колоноскопии и, таким образом, способствует предотвращению колоректального рака.
При описании качества подготовки BBPS считается наиболее тщательно проверенной шкалой [14] и предполагается, что она будет использоваться в клинических условиях для всех опубликованных шкал, показывающих ограничения [15]. Кроме того, если в рейтинге для каждой колоноскопии участвует более одного оценщика, может быть рекомендована дихотомическая конечная точка [16]. Поэтому в качестве основного результата мы использовали адекватную скорость подготовки кишечника. Все эндоскописты в текущем исследовании были хорошо обучены устранению предвзятости и использовали BBPS для оценки на основе своего собственного опыта.Более того, всестороннее рассмотрение общих и сегментарных показателей толстой кишки также оставалось хорошим способом подтверждения результатов сравнения различий в подготовке кишечника.
В включенных исследованиях индивидуально оценивалась эффективность адъювантных препаратов в снижении количества растворов препаратов для кишечника: одно — с прукалопридом [17], а остальные четыре — с бисакодилом [18–21]. В нашем обзоре подчеркнута возможность использования комбинации для подготовки кишечника после обобщения результатов (первичных или вторичных) у 1013 пациентов.Результаты не показали значительных недостатков в группе с меньшим объемом. В то время как для чистоты левой кишки Kang et al. [19] и Kim et al. [21] обнаружили, что прямая и сигмовидная кишка была более статистически эффективной в группе 1L PEG-AA (2,57 против 2,26). Помимо расхождений в статистических данных, были изучены источники неоднородности в рамках исследования, и было обнаружено, что это могло быть связано с добавлением разных количеств воды и дополнительным 1 л воды, введенным в качестве последней дозы по сравнению с 0.5 л в других исследованиях (). Было бы очень интересно оценить, может ли дополнительная вода без приема слабительного повлиять на чистоту кишечника. Другим объяснением может быть разница в дозировке и типе использования адъюванта.
Кроме того, на подготовку кишечника влияют многие факторы, связанные с пациентом, что неизбежно приводит к неоднородности. Как показали несколько предыдущих исследований, такие предикторы, как возраст, пол, ИМТ, предыдущая история колоноскопии, диетические ограничения, различие в марке лекарств, показания к проведению колоноскопии и интервал времени до процедуры, показали связь с очищением толстой кишки [22, 23 ].Почти все исследования, включенные в этот метаанализ, были внутренне согласованными в этих отношениях, чтобы исключить влияние этих смешивающих факторов на результаты. Тем не менее, в исследовании Кима наблюдалась статистически значимая разница в среднем возрасте пациентов [20]. Результаты нашего исследования показали, что пациенты в группе 2L (48,14 против 52,88) были моложе, что не соответствовало общепринятому пороговому значению, и результаты в конечном итоге не показали значительной разницы между двумя группами [22].
Тем не менее, в соответствии со стандартом подготовки кишечника, мы считаем, что достаточно балла BBPS ≥2 для всех сегментов и / или общего балла ≥ 6 [24]. Хотя в руководстве указано, что минимальный стандарт ≥90% для адекватной подготовки кишечника, оцененный с использованием проверенных шкал, может достичь только меньшинство центров, а в литературе указано, что уровень неадекватной подготовки кишечника в настоящее время составляет от 5% до 30%. [2, 25]. Уровень АД в этом исследовании с объединенным показателем 89% колебался от 83% до 96%, все из которых находились на среднем и верхнем уровне в клинической практике.Более того, показатели ADR и CIR были выше минимального стандарта (ADR ≥ 20%, CIR ≥ 90%) для колоноскопии в каждом испытании в соответствии с действующими рекомендациями (Таблица S4) [2]. Возможно, пока слабительное принимается в определенной дозе, другие аспекты, вызывающие беспокойство, а не доза, могут играть более важную роль в подготовке кишечника.
Еще одним заметным преимуществом этого протокола является готовность пациентов к повторению, набор достаточного количества пациентов и явно продемонстрированное предпочтение схемам с более низкими дозами [26].Режим с более низкими дозами, при котором большое количество раствора заменяется адъювантом за день до колоноскопии, особенно использование дополнительных суппозиториев в день колоноскопии, может уменьшить нарушение сна [20]. Во-вторых, он снижает потребление этих невкусных жидкостей, что может снизить психологическую нагрузку на пациентов. Желание пациентов должно быть высоко оценено, несмотря на одинаковые показатели завершения у пациентов, и не следует поощрять подход с высокой степенью подготовки для всех [27–29].
Осложнения пациентов в основном были связаны с наиболее частыми побочными эффектами, включая тошноту, рвоту, боль в животе и диарею [30]. Результаты этого исследования не показали статистических различий, в то время как можно сделать только консервативную оценку из-за ограниченного размера выборки в этой части. Основываясь на имеющейся в настоящее время литературе, наши результаты подтверждают использование дополнительных адъювантов только с раствором PEG-Asc [17–21]. Согласно гипотезе, катартическое действие бисакодила и прукалоприда может быть связано с его катарсическим или прокинетическим механизмом, который, в свою очередь, изменяет двигательные паттерны в толстой кишке и способствует движению кишечника [31, 32].
В настоящее время скорость адекватной подготовки кишечника значительно улучшилась клинически [29], но опыт приема слишком большого количества слабительных средств по-прежнему остается серьезной проблемой. Роль адъювантов в низком объеме PEG-Asc неясна, и в текущих рекомендациях говорится, что использование прокинетических агентов обычно не рекомендуется [5]. Таким образом, они не нашли широкого применения в повседневной клинической практике. Несмотря на ограниченное количество опубликованных данных в некоторых исследованиях, этот обзор свидетельствует об отсутствии очевидных недостатков в отношении эффективности и безопасности схем лечения 1 л ПЭГ-АА у амбулаторных пациентов.
Наш анализ включал нескольких пациентов, а также обнаружил приемлемую гетерогенность в большинстве сравнений по основным исходам. Следует отметить некоторые ограничения в этом исследовании. Во-первых, было включено меньшее количество исследований, и все исследования были взяты из одной страны; поэтому обобщаемость результатов сомнительна и требует дополнительных исследований для проверки результатов. Во-вторых, не все детали, представленные в этом исследовании, были проанализированы из-за ограниченной информации о вкусовых качествах и общем дискомфорте, которые могли иметь значение, но не иметь клинического значения.В-третьих, почти все включенные популяции были амбулаторными, и, учитывая эти ограничения, результаты нашего исследования следует применять с осторожностью. Согласно предыдущему исследованию, услуги амбулаторной помощи оставались фактором низкого риска, что указывает на то, что 1 л PEG-AA может быть более подходящим для населения с низким риском [33]. Наконец, в качестве вспомогательных препаратов использовались только бисакодил и прукалоприд, и необходимы дальнейшие исследования для изучения эффективности сочетания других препаратов, таких как пробиотики, мозаприд, цитрат магния и касторовое масло, с 1 л PEG-Asc.
http://ligadez.ru/index.html2020-03-21daily0.5http://ligadez.ru/images/doctor-563429.png.php2019-10-15daily0.5 http://ligadez.ru/tork-471110.php2019-10-15daily0.5 http://ligadez.ru/tork-471113. php2019-10-15daily0.5 http://ligadez.ru/tork-552000.php2019-10-15daily0.5 http://ligadez.ru / tork-552008.php2019-10-15daily0.5 http://ligadez.ru/tork-552100.php2019-10-15daily0.5 http://ligadez.ru/instrudes.php2019-03-18monthly0.5 http://ligadez.ru/tork-552100.php2019-10-15daily0.5 http://ligadez.ru/instrudes.php2019-03-18monthly0.5http: // ligadez.ru/images/instrudes.jpg
Новые рекомендации ВОЗ по предоперационным мерам профилактики инфекций в области хирургического вмешательства: глобальная перспектива, основанная на фактических данных
Ссылки
13 ноября 1976 г. · Британский медицинский журнал · SJ PowisD G Arkell
1 июля 1992 г. · The Journal of Hospital Инфекция · W LynchA Napier
1 августа 1989 · Европейский журнал сосудистой хирургии · JJ EarnshawB R Hopkinson
1 апреля 1988 · The Journal of Hospital Infection · LJ Hayek, JM Emerson
1 августа 1988 · The Journal of Больничная инфекция · ML Rotter
1 апреля 1985 г. · Британский журнал урологии · PE Randall Р. У. Маркусон
1 марта 1971 г. · Американский журнал хирургии · R Seropian, BM Reynolds
1 сентября 1982 г. · Журнал больничной инфекции · Дж. Х. Платт
, 1 сентября 1983 г. · Журнал больничных инфекций · Д. А. Ли Дж. Седжвик
1 сентября 1983 г. · Журнал больничных инфекций · Дж. Эйлифф Джексон
1 марта 1983 г. · Архив хирургии · Дж. У. Александер М. Дж.М. Оррис
1 марта 1983 г. · Американский журнал хирургии · П. Тур де Коос, Б. МакКомас
1 ноября 1994 г. · Британский журнал хирургии · JC SantosC E Levy
1 июня 1994 г. · Британский журнал хирургии · П. Берк Дж. Хайленд
1 мая 1997 г. · Инфекционный контроль и больничная эпидемиология: официальный журнал Общества эпидемиологов больниц Америки · М. Лизан-ГарсияА Асенсио-Вегас
16 июня 1999 г. · Ларингоскоп · СН Снайдерман Р. Рюгер
29 декабря 1999 г. · Журнал торакальной и сердечно-сосудистой хирургии · WE TrickW R Jarvis
9 февраля 2000 г. · Хирургия сегодня · Y TakesueY Matsuura
29 мая 2000 г. · Заболевания толстой и прямой кишки · RP MiettinenM E Pääkkönen
15 февраля 2001 г. · Annals of Rheumatic Diseases · DM GrennanS Fear
12 сентября 2001 г. · Lancet · R TepaskeJ Kesecioglu
5 января 2002 г. · Хирургия сегодня · H IshidaD Hashimoto
30 июля 2002 г. · Клинические инфекционные заболевания: Официальная публикация инфекции Общество болезней Америки · Доктор медицины KalmeijerJ AJW Kluytmans
10 августа 2002 г. · JAMA: Журнал Американской медицинской ассоциации · Жан Жак ПариентиУЗНАНО Antisepsie Chirurgicale des main Study Group
13 ноября 2002 г. · Европейский журнал клинического питания · DA de LuisM C Terroba
5 декабря 2002 г. · Журнал AORN · Синтия Г. Сигал, Жаклин Дж. Андерсон
13 мая 2004 г. · Европейский журнал клинического питания · DA de LuisR Aller
22 апреля 2005 г. · Международный журнал колоректальных заболеваний · Элой Эспин-Басани, Мануэль Арменгол-Карраско,
,, 28 июня 2005 г. · Заболевания толстой и прямой кишки · Патрик Фа-Си-Оэн, Фред Круазет ван Учелен,
,, 30 июня 2006 г. · Журнал антимикробной химиотерапии · Кевин В.
26 августа 2006 г. · Журнал больничных инфекций · A KonvalinkaI W Fong
24 ноября 2006 г. · Хирургия сегодня · Hisanaga HorieHideo Nagai
16 декабря 2006 г. · Хирургия основания черепа · MA HorganJ B Delashaw
8 марта 2007 г. · Клинические инфекционные заболевания: официальная публикация Общества инфекционистов Америки · Марджо Э. ван Кастеренинге К. Гиссенс
28 апреля 2007 г. · JPEN.Журнал парентерального и энтерального питания · Роберт ТепаскеМаргрит Врум
1 мая 2007 г. · Хирургия сегодня · Минако КобаяшиНЕИЗВЕСТНО Группа исследований хирургической инфекции Ми
22 мая 2007 г. · Британский журнал хирургии · B JungUNKNOWN
Группа исследования механической подготовки кишечника 11, 2007 · Позвоночник · Суат Э Челик, Айхан Кара19 сентября 2007 · Всемирный журнал хирургии · Хироя ТакеучиСумио Мацумото
25 декабря 2007 · Ланцет · Кэролайн МЭ ContantWibo F Weidema
4 июня 2008 · Annals of Хирургия · Уолтер П. ВеберАндреас Ф. Видмер
23 августа 2008 г. · Журнал гастроэнтерологии и гепатологии · Такехиро ОкабаяшиКазухиро Ханазаки
17 сентября 2008 г. · Архив хирургии · Ширин ТовфайСэмюэль Э Уилсон
· 31 октября 2008 г. · Пластическая хирургия и реконструктивная хирургия Даниэла Ф Вейга Лидия М Феррейра
3 декабря 2008 г. · Инфекционный контроль и больничная эпидемиология: официальный журнал Общества эпидемиологов больниц Америки · Даниэла Фра ncescato VeigaЛидия Масако Феррейра
11 июня 2009 г. · Инфекционный контроль и больничная эпидемиология: Официальный журнал Общества эпидемиологов больниц Америки · Дидье Питтет НЕИЗВЕСТНО Всемирная организация здравоохранения Всемирный альянс за безопасность пациентов Первый глобальный вызов безопасности пациентов Основная группа экспертов
23 июля 2009 г. · BMJ: Британский медицинский журнал · Алессандро ЛибератиДэвид Мохер
5 августа 2009 г. · Журнал костной и суставной хирургии.Американский том · Мэтью Д. Зальцман · Джейсон Л. Ко
3 октября 2009 г. · Foot & Ankle International · Кеннет Ченгиан МакЛеод
8 января 2010 г. · Медицинский журнал Новой Англии · Лоннеке GM BodeMargreet C Vos
Цитирования
7 ноября 2016 г. · Инфекционные заболевания Lancet · Benedetta Allegranzi НЕИЗВЕСТНО Группа разработки рекомендаций ВОЗ23 февраля 2017 г. · Радиационные исследования · Мануэла Буонанно, Дэвид Дж. Бреннер
8 апреля 2017 г. · The Lancet Infectious Diseases · Хилари Хамфрис, 28 апреля 2017 г. · Хирургические инфекции · Stijn W de JongeMarja A Boermeester
25 марта 2018 г. · Журнал хирургической онкологии · Xiang-Dong WuWei Huang
21 февраля 2018 г. · Хирургические инфекции · Juyuan LiuMeng Cai
7 февраля 2018 г. · Кокрановская база данных систематических обзоров · Zhenmi LiuHung-Yuan Cheng
30 марта 2018 г. · Журнал AORN · Raelina S HowellScott Gorenstein
13 апреля 2018 г. · Фармацевтические исследования · Eduardo Celia PalmaTeresa Dalla C osta
14 октября 2017 г. · Европейский журнал кардио-торакальной хирургии: Официальный журнал Европейской ассоциации кардио-торакальной хирургии · Мигель Соуза-УваУльф Ландмессер
11 ноября 2017 г. · Экспертный обзор противоинфекционной терапии · Семь Йоханнес Сэм Агдасси, Петра Гастмайер
30 марта 2018 г. · Журнал эстетической хирургии · Никки К. ГирсФранк Б. Ниссен
13 декабря 2017 г. · Анестезиология · Кристиан С. МейхоффГоран Хеденшерна
10 июля 2018 г. · CA: Онкологический журнал для клиницистов · Элла Дж. Ариса-Эредиа, Рой Ф. Чемали
20 июля 2018 г. · Журнал оценки в клинической практике · Шейла Калб Вайнберг Даниела Оливейра де Мело
15 мая 2018 г. · Анестезия и обезболивание · Леон Воробейчик Джордан Таршис
24 июля 2018 г. Журнал Американской академии хирургов-ортопедов · Эна Нильсен, Дэвид Л. Скэггс
9 сентября 2017 г. · Хирургические инфекции · Вики Стругала, Робин Мартин
15 июня 2017 г. · Хирургические инфекции · Сон Лю Цзяньань Рен 900 03
29 августа 2018 · Технологии и терапия диабета · Юки СугиямаМикито Кавамата
19 августа 2017 · Журнал материнско-фетальной и неонатальной медицины: Официальный журнал Европейской ассоциации перинатальной медицины, Перинатальной Федерации Азии и Океании Общества, Международное общество перинатальных акушеров · Huaping HuangMei He
21 сентября 2018 г. · Британский журнал медсестер: BJN · Мел Бёрден, Мелани Торнтон
14 июня 2017 г. · Противомикробные препараты и химиотерапия · Дерри К. Мерсер Дебора А О’Небора
10 января 2018 · Ларингоскоп · Margeaux CorbyStephen Park
1 сентября 2017 · Анналы хирургии · Виллем-Ян Метсемакерс Альберт Вольтуис
6 ноября 2018 · Экспертный обзор противоопухолевой терапии · Майнул ХакМассимо
2018 · Журнал антимикробной химиотерапии · DPR TroemanJ AJW Kluytmans8 ноября 2017 · Анналы хирургии · Арвид Стейнар ХаугенEirik Søfteland
6 февраля 2018 · Анналы клинической микробиологии и противомикробных препаратов · Сюй Ян Хуанань Ван
14 января 2018 г. · Исследования костей и суставов · STJ TsangK E Templeton
7 марта 2019 г. · Хирургические инфекции · Мануэль Лопес-КаноДж М. Гарсия-Аламино
7 марта 2019 г. Интерактивный журнал медицинских исследований · Вахби АльбишиСалех Алдакал
15 марта 2019 г. · International Wound Journal · Джошуа П. Тоттиян С. Четтер
19 февраля 2019 г. · Инфекционный контроль и больничная эпидемиология: Официальный журнал Общества эпидемиологов больниц Америки · Didier Lepelletier НЕИЗВЕСТНО Рабочая группа французского общества больничной гигиены
5 апреля 2019 г. · Инфекция · Себастьян Блатт, Билал Аль-Навас
27 апреля 2019 г. · Журнал AORN · Шарль Эдмистон Карен Труит
10 мая 2019 г. · PloS One · Hui ЧжаКоичи Юки
17 сентября 2018 г. · Всемирный журнал урологии · Ханан ГолдбергОфер Йосепович
19 июня 2019 г. · Europace: Европейская кардиостимуляция, аритмии и электрофизиология сердца: журнал Рабочие группы по кардиостимуляции, аритмиям и клеточной электрофизиологии Европейского общества кардиологов · Васил Трайков · Карина Бломстрём-Лундквист
30 мая 2019 · Противомикробные препараты и химиотерапия · Roger V AugtinesLloyd S Miller
, 2019 · Элизабет Кэрролл, Ариан Льюис8 августа 2019 г. · Дерматология JAMA · Харви СмитКарл Винчиулло
9 августа 2019 г. · Оценка медицинских технологий: HTA · Barnaby C ReevesJane M Blazeby
13 июля 2019 г. · Клинические инфекционные заболевания: официальный Публикация Общества инфекционистов Америки · Джозеф С. Соломкин
31 июля 2019 г. · Больничная практика · Пинки Мпинда-Джозеф Брайан Годман
27 сентября 2019 г. · PloS One · Росселла ЗуккоAida Bianco
2 октября 2019 г. · Будущая микробиология · Джозеф С Соломкин Ларри Цай
9 ноября 2019 · Открытие сети JAMA · Кортни Иерано Триша Пил
15 октября 2019 · Анестезия и обезболивание · Джиа Л. Стивенс Дэниел С. Март в
25 июля, 2019 · Безопасность пациентов в хирургии · Кидани ФишаКоку Сисай Тамират
Что и как правильно дезинфицировать обувь после грибка
Эта обработка проводится специальными растворами и спреями.Кроме того, могут помочь специальные инструменты, которые могут воздействовать на споры ультрафиолетом.
Средство дезинфекционное
В любом крупном городе есть магазины дезинфицирующих средств, медицинской химии, профессиональной химии. Их можно найти в региональных справочниках или в Интернете. Пример .
В таблице ниже приведен список дезинфицирующих средств, подходящих для дезинфекции обуви, их концентрация и продолжительность замачивания.
Отбираются только те средства, для которых в официальной инструкции четко указано «Обработка обуви из кожи и кожзаменителя», «Лечение от кандидоза и дерматофитов»:
| Название | Концентрация | Пример разбавления | Время выдержки | Ссылка на официальную инструкцию |
| A-des | 1% | 100 мл препарата на 10 л воды | 15 минут | |
| Абсолютид Дикват | 1% | см. Выше | 60 минут | |
| Abacteril | 1% | см. Выше | 30 минут | HTML |
| Альпиника | 5% | 0.5 литров препарата на 9,5 литров воды | 30 минут | |
| Ник Неодез * | 3,5% | 350 мл препарата на 10 л воды | 60 минут | 1 и 2 |
| Ultima | 2% | 200 мл препарата на 10 л воды | 30 минут |
Распечатать таблицу
Необходимо приготовить раствор этой концентрации и замочить в нем обувь на время, указанное в таблице.После замачивания тщательно промойте обувь в чистой воде и просушите.
Как это сделать: подробный фотоотчет.
Примечание (*): Nick — это довольно популярная и очень широкая линейка инструментов. К обуви подходит только «Ник Неодез».
Концентрированное дезинфицирующее средство может быть довольно агрессивным, не допускайте попадания его в глаза или рот, после использования вымойте руки с мылом. В случае попадания в глаза немедленно промойте большим количеством воды и обратитесь в ближайшую приемную комиссию.При случайном проглатывании необходимо промыть желудок, а также обратиться к врачу.
Хлоргексидин
Для дезинфекции обуви подходит хлоргексидина биглюконат, , но только в концентрации 1% . Эффективен против дрожжей и дерматофитов. Хлоргексидин не имеет цвета и запаха, поэтому пользоваться им очень удобно. Единственный недостаток — достать непросто. В аптеках продают 0,05%, потому что в более высокой концентрации он опасен для слизистых оболочек и т. Д.
Как дезинфицировать обувь от грибка: смочите в растворе ватный тампон и протрите им всю внутреннюю поверхность обуви, уделяя особое внимание труднодоступным местам. Далее обработанную обувь складывают в полиэтиленовый пакет, плотно завязывают и оставляют на 3-4 часа. По их истечении 2-3 дня отводится на просушивание обуви.
Полная инструкция
Вы можете купить в магазинах дезинфицирующих средств, смотрите наш фотоотчет.
Синоним 1% хлоргексидина — Desiheend , он, как и хлоргексидин , можно найти в магазинах медицинской техники, медицинской химии, профессиональной дез. Означает .
Используйте 1% раствор только для дезинфекции обуви и поверхностей.Для полосканий, так же для обработки половых органов и открытых ран предназначен раствор 0,05%!
Микостоп
Спрей от грибка для обуви «Микостоп» очень удобен. Его распыляют на ночь на внутреннюю поверхность обуви в течение 3-5 дней. Противогрибковую обработку следует проводить для всех пар обуви, которые использовались после обнаружения грибка и во время его обработки.Учтите, что средство от грибка обуви на основе ундециленамина эффективно против всех грибков, ответственных за возникновение грибковых инфекций. Подробнее ..
Мирамистин
Достаточно известное универсальное антибактериальное средство. Продается в аптеках.
Используется как местный антисептик, практически без запаха, но стоит немало, учитывая, сколько на него придется потратить даже на пару обуви. В этом смысле наиболее выгодный вариант — флакон на 500 мл.Продается нечасто, но выгоднее бутылочек.
Полная инструкция, цена, где купить.
Используйте 0,1% раствор — тщательно смочите ватный / марлевый тампон и пропитайте всю внутреннюю поверхность обуви. После этого дайте обуви высохнуть.
Дезавид
Средство уничтожает грибы рода Candida и грибы-дерматофиты, плесневые грибы. Это исключает рецидив болезни из-за собственной загрязненной обуви. Дезавид также устраняет неприятные запахи и является мощным антисептиком.
Выпускается в форме спрея во флаконе 150 мл. Цена 200-300 руб. В магазинах бытовой химии.
Достоинств:
- Гипоаллергенный препарат (среди компонентов нет отдушек, спирта и хлора).
- Подходит для обуви из любых материалов, в том числе из кожи и замши.
- Не имеет запаха.
- Не оставляет следов.
Способ применения:
Вариант 1.Обильно смочите тряпку или ватный тампон спреем и протрите внутреннюю поверхность обуви.
Вариант 2. Распылите «Десавид» с расстояния 30 см на внутреннюю поверхность обуви. Время выдержки 3-5 минут. Как только средство высохнет, обувь можно использовать по прямому назначению.
Во время лечения противогрибковыми средствами обработка обуви спреем от грибка ногтей должна быть ежедневной.
Лаина
Прозрачная жидкость синего или зеленого цвета с запахом активна в отношении грибов рода Trichophyton (дерматофиты), Candida, плесневых грибов.Выпускается в виде раствора во флаконах и канистрах емкостью 0,5 л, 1,0 л, 5 л и 10 л.
Часто продается в ветеринарных аптеках.
Запрещается использовать обувь белого цвета, а для обуви светлых тонов!
Способ применения:
Обувь протирают дважды тампоном, плотно смоченным в растворе. По истечении определенного времени внутренняя поверхность обрабатывается водой и сушится. Тапочки, банные сандалии и прочая обувь этого типа дезинфицируются погружением в раствор Лайне и создают препятствия для их подъема.Затем обувь ополаскивается водой.
Внимание! Концентрация раствора для дезинфекции обуви от грибковых инфекций составляет 0,5% и 0,8%. Обработка обуви при грибке стоп составляет 30 и 15 минут соответственно.
Формалин
У этого средства очень резкий запах, что, несомненно, является его самым большим недостатком, но не главным. Иногда советуют использовать его для дезинфекции обуви, но помните, что вещество канцерогенное, а токсично.При постоянном применении отрицательно влияет на центральную нервную систему, репродуктивные органы, дыхательные пути, слизистые оболочки, кожу.
Бицин
Запатентованный нанокомплекс, который защищает обувь от грибка на 20-40 дней, уничтожает резкий запах пота, уничтожает вредные бактерии и споры грибов Candida, плесени и дерматофитов. В комплект входят: концентрат концентрата в пластиковой ампуле, пульверизатор с подготовленной водой. Приготовленный раствор может храниться до 5 лет.
Как обращаться с обувью после грибка? В бутыль с подготовленной водой слить весь концентрат из ампулы, затянуть и 5-6 раз встряхнуть. Готовый раствор распыляется на внутреннюю поверхность обуви. Разрешается распылять Бицин на мокрую обувь. Обувь можно носить сразу после лечения. Набора хватает на 2-3 процедуры.
Продается в аптеках, хотя найти непросто. Также его можно продавать в магазинах для туристов, охотников и рыбаков.
Иногда рекомендуется использовать уксус для дезинфекции обуви, но имейте в виду, что он имеет сильный запах, который очень трудно удалить. Возможно, вам не захочется носить обувь после такой дезинфекции.
Аламинол
Концентрат «Аламинол» разводят 1: 100 или 5: 100 (получается либо 1%, либо 5% раствор). Полученный раствор заливается в обувь и сразу же выливается. Влажную обувь оставляют на 1,5 часа, а затем дважды ополаскивают водопроводной водой. После высыхания обувь можно носить.
Этот же раствор используется для замачивания стелек.
Литровая жидкость стоит 300-500 руб., Продается в специализированных магазинах медицинских товаров и дез. Средства.
Аппараты для дезинфекции обуви
Дезинфекцию обуви от грибка можно проводить и специальными ультрафиолетовыми приборами. Они убивают споры грибов и бактерий, но не представляют опасности для домашних животных и человека. Некоторые модели не только дезинфицируют, но и сушат обувь.
ТИМСОН . Согласно независимым (?) Исследованиям, устройство, если его включить на 6-8 часов и поместить внутрь обуви, уничтожает 100% грибов Candida, 99,67% грибов Trichophyton rubrum и 99,87% грибов рода Trichophyton mentaqrophytes.
Оставим вопросы по точности исследований, так как УФ-излучение уничтожает грибок, это стопроцентный факт.
Пользоваться очень просто: прибор кладется в каждый носок обуви на 6-12 часов.В это время на споры грибка в обуви воздействуют четыре ультрафиолетовых лампы, встроенные по периметру.
КСЕНЕЛИТ . Ультрафиолет этого устройства воздействует на ДНК грибов и убивает их на 99,9%. В инструкции написано, что обработка обуви от грибка займет 5 минут, поэтому за час можно продезинфицировать обувь всех членов семьи.
Внутри Ксенелайта установлены газоразрядные бактерицидные лампы. Вместе с устройством в обувь помещается осушитель.Внимание! Для сушки необходимо оставить в обуви влагопоглотители на 4-6 часов. Устройство подходит для домашней, спортивной и модельной обуви. Втыкать в розетку необязательно: работает от 4-х батареек ААА (соответственно на пару обуви потребуется 8 батареек). Они длятся 2 месяца. В общей сложности устройство должно проработать 5-7 лет.


 ч. однократного применения.
ч. однократного применения. [19], 2017 (Корея)
[19], 2017 (Корея) 07
07 69
69